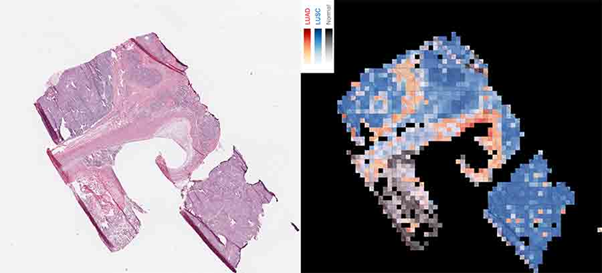
Ảnh: Chương trình máy tính sử dụng trí tuệ nhân tạo phân tích mẫu mô bằng cách tạo ra một bản đồ với hàng ngàn ô vuông siêu nhỏ. Bản đồ bên phải cho thấy ung thư biểu mô tế bào vảy (màu đỏ), ung thư biểu mô tế bào vảy của phổi (xanh) và mô phổi bình thường (xám)
Tác giả: Dương Thị Nhung
Trường Đại học Nghiên cứu Quốc gia về Hạt nhân “MEPhI” (Liên bang Nga)
Email: duongthinhung_t57@hus.edu.vn
Như chúng ta đã biết, hiện nay cả thế giới đang đứng trên cuộc cách mạng công nghiệp 4.0 và trí tuệ nhân tạo biết đến như chiếc chìa khóa để biến những ý nghĩ của con người thành hiện thực. Mới đây, các nhà nghiên cứu từ Trung tâm Y tế Langone, thuộc Đại học New York (New York University - NYU) đã tạo ra một chương trình máy tính để “đọc” các tiêu bản cho việc chẩn đoán hai loại ung thư phổi phổ biến nhất với độ chính xác lên đến 97%. Chương trình cũng đã được nghiên cứu để phát hiện đột biến di truyền liên quan đến ung thư trong các mẫu chỉ bằng cách phân tích các hình ảnh của các mô khối u.
Như các hệ thống xử lý dữ liệu khác được thiết lập dựa trên cơ sở của công nghệ "Máy học" (Machine Learning), chương trình máy tính sẽ quét qua hình ảnh các lát cắt của mô và phát triển khả năng phân biệt mô phổi bình thường với hai loại ung thư phổ biến nhất là ung thư biểu mô tuyến - adenocarcinoma (chiếm khoảng 40%) và ung thư biểu mô tế bào vảy - Squamous adenocarcinoma (25% đến 30%). Ngay cả các nhà giải phẫu bệnh giàu kinh nghiệm cũng gặp nhiều khó khăn khi phân biệt hai loại ung thư này để lập phác đồ điều trị.
Để tạo ra chương trình, các nhà nghiên cứu về máy học đã sử dụng phương pháp học tập sâu -Deep learning method, được phát triển và phát hành bởi Google. Chương trình sử dụng trí tuệ nhân tạo (Artificial Intelligence-AI) để tự dạy chính mình nhằm đạt được kỹ năng tốt hơn và được tạo ra dựa trên hơn 1600 mẫu mô bệnh học ung thư phổi được công bố trên Bản đồ gen ung thư (The Cancer Genome Atlas - TCGA). Nghiên cứu được thực hiện bởi các nhà khoa học từ Trung tâm Y tế Langone thuộc NYU và được công bố vào ngày 17 – 9 - 2018 trên Nature Medicine. Kết quả cải thiện đáng kể độ chính xác về phương pháp chẩn đoán ung thư phổi với tỷ lệ chính xác là 83%.
Các hình ảnh dưới dạng dữ liệu và nguồn thông tin chung
TCGA thiết lập hình ảnh mô bệnh học của các mẫu khối u bằng một tiêu chuẩn kiểm soát chất lượng cho việc nghiên cứu chuỗi dữ liệu di truyền được thu thập trong dự án. Ông Jean C. Zenklusen, tiến sĩ, giám đốc của TCGA tại Viện ung thư Quốc gia Mỹ (National Cancer Institute-NCI) nói: “Những hình ảnh cần đảm bảo chất lượng và nhận dạng mô phải chính xác vì nó là nguồn dữ liệu để phân tích”. Chúng có độ phân giải cao nên các nhà nghiên cứu tại NYU có thể chia thành hàng ngàn ô nhỏ hay các “miếng vá” để chương trình máy tính có thể phân tích một cách riêng rẽ, cung cấp tín hiệu trực quan và phân loại. Narges Razavian, Tiến sĩ tại NYU Langone: “Chúng tôi có khoảng 500 bệnh nhân trên mỗi loại ung thư phổi và tiến hành hàng ngàn “miếng vá” cho mỗi mẫu, vì vậy chúng tôi có hàng triệu “miếng vá” để phát triển mô hình”.
Độ chính xác mà chương trình “học” được để phân biệt ung thư biểu mô tuyến với ung thư biểu mô tế bào vảy và tế bào phổi thông thường tương đương với các nhà giải phẫu bệnh giàu kinh nghiệm. Kết quả phân tích của chương trình có thể nhanh hơn rất nhiều và có thể đạt được kết luận chỉ trong vài giây thay vì vài phút như các nhà giải phẫu bệnh cần. Chương trình cũng đã phân loại chính xác 45/54 hình ảnh mà đã có ít nhất 1 trong 3 nhà giải phẫu bệnh tham gia nghiên cứu phân loại sai.
Chương trình đã được kiểm tra trên tập hợp các mẫu ung thư phổi độc lập - tất cả đều được đông lạnh và mới được thu thập từ NYU, để xác minh rằng nó đã hoạt động dựa trên các mẫu thu thập hoàn toàn riêng biệt. Các mẫu của TCGA gần như hoàn toàn là các mô khối u. Tuy nhiên các mẫu thường bao gồm các thành phần khác như cục máu đông, mô chết và những thành phần này khiến cho việc phân loại trở nên khó khăn hơn cho chương trình. Để khắc phục điều này, các nhà nghiên cứu đã lập trình lại chương trình để nó tập trung phần lớn vào phần mẫu được coi là u (được xác định bởi nhà nghiên cứu bệnh học). Với việc thay đổi này, độ chính xác trung bình của phương pháp lớn hơn 90%. Đây là một kết quả rất đáng khích lệ.
Vai trò của AI trong điều trị và nghiên cứu
Do chương trình có tốc độ nhanh và độ chính xác cao, nhóm nghiên cứu đã đề xuất công cụ này có thể được sử dụng trong quá trình phẫu thuật. Ví dụ: để xác minh rằng mẫu bệnh phẩm lấy từ khối u trong quá trình phẫu thuật có đủ chất lượng để chẩn đoán hay không hoặc để thông báo cho bác sĩ phẫu thuật lấy một mẫu khác nếu cần thiết.
Ngoài việc chỉ ra rằng AI có thể được sử dụng để chẩn đoán một cách nhanh chóng và chính xác, dự án này còn cho thấy AI có thể được lập trình để dự đoán sự hiện diện của 6 đột biến di truyền phổ biến nhất trong ung thư biểu mô tuyến ở phổi. Độ chính xác dao động từ 64-86%, phụ thuộc vào gen.
Hiện tại, cách duy nhất để con người có thể phát hiện đột biến di truyền là việc xác định sự sắp xếp DNA, điều này có thể mất đến 2 tuần. Tiến sĩ Razavian cho biết thêm: “Ung thư phổi thường được phát hiện muộn vì bệnh nhân phải đợi đến 2 tuần để bắt đầu điều trị, điều này nguy hiểm vì quá trình tiến triển nhanh của bệnh”.
Nhiều đội y tế sẽ bắt đầu việc điều trị và sau đó kê đơn thuốc sử dụng dựa trên kết quả xét nghiệm di truyền. Tiến sĩ Razavian nói: “Với chương trình này, chúng ta có thể bắt đầu điều trị gần như ngay lập tức”.
Chương trình được coi là “hộp đen” vì sự giải quyết của nó là kết quả của hàng nghìn bước nhỏ liên tiếp. Chương trình có thể phát hiện những điều bất thường trong hình ảnh cung cấp, cái mà ngay cả những nhà giải phẫu bệnh cũng khó có thể hình dung được một cách chính xác, nhằm dự đoán sự hiện diện của đột biến di truyền. Do đó có thể coi chương trình như là “một ống kính để xem xét các mô khi khó nhận thấy bằng mắt”
Tiến sĩ Razavian và các cộng sự của mình sử dụng chương trình để nghiên cứu về việc làm thế nào mà đột biến di truyền ảnh hưởng lên cấu trúc của tế bào và các mô. Để tiếp cận vấn đề này, họ sử dụng phương pháp tự động sửa đổi hình ảnh để tìm ra yếu tố nào ảnh hưởng nhiều nhất đến khả năng nhận biết đột biến của chương trình.
Paula Jacobs, Tiến sĩ, Phó Giám đốc Chương trình hình ảnh ung thư của NCI cho hay: “Điểm mấu chốt của nghiên cứu là việc lựa chọn cẩn thận đối tượng lâm sàng để giải quyết”, chương trình đã được lập trình và thực tế là các kết quả của nó được kiểm tra bằng cách sử dụng bộ đọc độc lập với các mẫu ung thư phổi.
Tiến sĩ Michael Snyder, chủ tịch di truyền học tại Đại học Stanford, nhận thấy AI là tương lai của chẩn đoán. Ông cho biết: “ Tôi nghĩ rằng chúng ta nên chuyển sang máy học chứ không nên chỉ dựa trên các nhà giải phẫu bệnh để làm tất cả công việc. Các thuật toán sẽ giúp các nhà giải phẫu bệnh trong việc phân loại và làm giảm các lỗi mà họ mắc phải”.
Chương trình này đã được phát triển cho các dự án có sẵn trong việc ứng dụng vào chẩn đoán. Đội của NYU đã bắt đầu áp dụng chương trình này để tìm hiểu cho việc chẩn đoán ung thư thận, vú, và các loại ung thư khác.
Tham khảo: NCI Staff (10/2018) Using Artificial Intelligence to Classify Lung Cancer Types, Predict Mutations. Available at: https://www.cancer.gov/news-events/cancer-currents-blog/2018/artificial-intelligence-lung-cancer-classification


