Trần Thanh Long
Phòng thí nghiệm công nghệ sinh học phân tử, khoa Sinh học-Công nghệ Sinh học, đại học khoa học Tự Nhiên tp HCM.
1. Mối đe dọa của sốt rét
Lây nhiễm cho 212 triệu người và gây ra cái chết của 429 nghìn người trong năm 2015 (theo thống kê của WHO) [1], sốt rét có lẽ là một trong những căn bệnh truyền nhiễm khét tiếng nhất ở các nước nhiệt đới và cận nhiệt. Không những chết người và có khả năng lây lan rộng, sốt rét từ lâu còn song hành với đói nghèo và tổn hại kinh tế: chỉ tính riêng ở châu Phi, hằng năm, căn bệnh này đã gây thiệt hại khoảng 12 tỉ dollar do chi phí chăm sóc, phục hồi sức khỏe; suy giảm năng suất lao động và tác động tiêu cực đến du lịch [2].
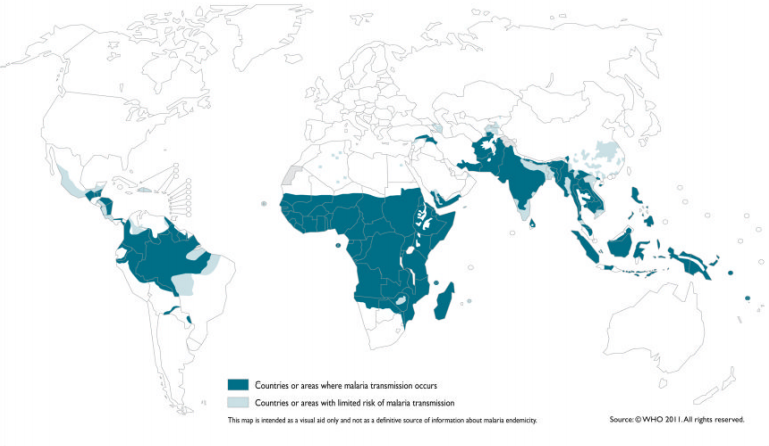
Hình 1: Các quốc gia và vùng lãnh thổ bị ảnh hưởng bởi sốt rét. Vùng màu xanh đậm: các khu vực đang có sự lan truyền sốt rét. Vùng màu xanh nhạt: các khu vực có nguy cơ lan truyền bệnh sốt rét.
Cũng như bệnh mù sông, nguyên nhân của sốt rét là do sự xâm nhiễm của kí sinh trùng. Các kí sinh trùng sốt rét thuộc họ Plasmodium (họ này có hơn 250 loài trong đó có 5 loài có khả năng lây truyền ở người là P. falciparum, P. malariae, P. ovale, P. vivax và P. knowlesi) xâm nhập cơ thể nạn nhân khi côn trùng mang mầm bệnh (muỗi cái Anopheles) hút máu họ. Trong số năm loài Plasmodium gây bệnh ở người, Plasmodium falciparum (P. falciparum ) là loại phổ biến nhất (nguyên nhân của khoảng 75% trường hợp bị sốt rét) [1] [3], và cũng là nguy hiểm nhất-hầu hết các trường hợp tử vong vì sốt rét là do P. falciparum. Nguyên nhân chính P. falciparum nguy hiểm hơn các loài trùng sốt rét có họ hàng gần của chúng là bởi khả năng phân chia với tốc độ rất nhanh trong cơ thể bệnh nhân: giai đoạn cư trú trong gan sau khi xâm nhiễm từ muỗi chỉ khoảng 5-7 ngày so với từ 8-16 ngày đối với các loài Plasmodium gây bệnh còn lại. Từ mỗi tế bào gan của bệnh nhân sẽ giải phóng ra khoảng 30.000 tế bào P. falciparum, gấp 3 lần ở các loài bà con của chúng (~10.000 tế bào kí sinh trùng/tế bào gan). Tổng số tế bào kí sinh trùng tối đa trong cơ thể bệnh nhân nhiễm P. falciparum có thể lên đến 2.000.000 tế bào/µl máu so với từ 20.000 đến trên 200.000 tế bào/µl máu ở các bệnh nhân nhiễm các loài Plasmodium gây bệnh khác) [1] [2] [4] [5] [6]. Khác với giun tròn gây bệnh mù sông là một loài động vật đa bào, kí sinh trùng Plasmodium (vi sinh vật đơn bào) nhỏ hơn rất nhiều (khoảng 100 lần) nhưng ở trường hợp của hai loài này, kích thước tỉ lệ nghịch với mức độ nguy hiểm (kích thước của kí sinh trùng sốt rét là khoảng 10 µm trong khi ấu trùng giun tròn Onchocerca volvulus đã dài tới 300 µm (1 mm = 1000 µm) còn con cái trưởng thành có thể có kích thước đến hơn nửa mét). Người bị nhiễm giun kí sinh O. volvulus tuy có nguy cơ bị tác hại xấu nhất là mù lòa nhưng hiếm khi nguy hiểm đến tính mạng. Còn đối với sốt rét, tử thần luôn sẵn sàng chực chờ mọi nạn nhân.
Hãy thử tưởng tượng bạn đang sống ở một nước nhiệt đới vào khoảng những năm 60 của thế kỉ trước. Vào một ngày đáng nhớ (hoặc đáng quên) bạn cảm thấy hơi ngứa ở cánh tay và phát hiện thấy một vết muỗi đốt, như vố số lần bị muỗi đốt trước đây, bạn không mấy bận tâm và quên ngay sau đó. Tuy nhiên, tại thời điểm bạn bị muỗi đốt, các kí sinh trùng Plasmodium, xâm nhập vào muỗi từ máu một bệnh nhân bị muỗi đốt trước đó, đang tập trung ở tuyến nước bọt, chuẩn bị sẵn sàng cho đợt xâm lượt kế tiếp. Các kí sinh trùng sau đó theo nước bọt của muỗi xâm nhập vào hệ tuần hoàn của người, ở giai đoạn này chúng được gọi là thoa trùng (sporozoite). Sau khoảng nửa giờ từ lúc xâm nhập, những thoa trùng với kích thước chỉ khoảng 10 µm (tám lần nhỏ hơn đường kính một sợi tóc) theo máu tới gan. Chúng sẽ cư ngụ ở đây khoảng từ 5 ngày đến một tuần, tăng trưởng và sinh sản vô tính để tạo ra hàng ngàn mảnh trùng (merozoite). Sau khi được giải phóng, các mảnh trùng xâm nhập vào hệ tuần hoàn và sau đó là hồng cầu. Tại đây, chúng sử dụng các phân tử hemoglobin (là những phân tử giúp hồng cầu vận chuyển Oxi khắp cơ thể) như nguồn cung cấp dinh dưỡng. Các mảnh trùng sau đó tiếp tục phân chia nhiều tới mức phá vỡ hồng cầu và thoát ra ngoài và tìm đến những hồng cầu xung quanh. Cứ thế, các mảnh trùng tăng sinh theo cấp số nhân, xâm nhập và phá hủy vô số tế bào máu (4-36 mảnh trùng được giải phóng từ một hồng cầu sau khoảng 48 giờ kể từ lúc xâm nhiễm hồng cầu), đây cũng là nguyên nhân trực tiếp dẫn đến triệu chứng của sốt rét [1] [2] [4]. Một số mảnh trùng không sinh sản vô tính như trên mà phát triển thành các giao bào (gametocyte) đực và cái, nằm chờ trong hồng cầu cho đến khi một muỗi cái Anopheles khác hút máu của bạn. Khi các hồng cầu nhiễm đi vào cơ thể muỗi cái, giao bào đực và cái thoát khỏi hồng cầu, tìm đến nhau và hợp thành trứng và sau đó lại nở ra hàng ngàn mảnh thoa trùng, sẵn sàng cho nạn nhân mới. Quá trình mảnh trùng xâm nhập và phá hủy hồng cầu cũng là lúc những triệu chứng tồi tệ và nguy hiểm đến với bạn: đau đầu dữ dội, sốt, đau khớp, nôn, ớn lạnh, vàng da,… (những triệu chứng đầu tiên này có thể bắt đầu xuất hiện từ ngày thứ bảy tính từ khi kí sinh trùng xâm nhập nhưng thông thường là từ 10-15 ngày). Nguy hiểm hơn cả là khi bệnh chuyển sang giai đoạn sốt rét ác tính với các triệu chứng nghiêm trọng hơn như rối loạn ý thức, hôn mê, co giật, thiếu máu nặng, suy hô hấp, suy thận, suy tuần hoàn, xuất huyết dưới da, cơ (việc chuyển sang giai đoạn nặng như trên có thể xảy ra rất nhanh nếu không được chữa trị trong khoảng 24 giờ từ khi xuất hiện các triệu chứng ban đầu) [7]. Ngay khi các triệu chứng trở nên nghiêm trọng khiến mọi sinh hoạt hàng ngày bị rối loạn, bạn lập tức tìm đến bác sĩ và nhận được kết quả chẩn đoán mình bị sốt rét. Tuy là một căn bệnh nguy hiểm, cả bạn và bác sĩ đều không quá lo lắng vì các thuốc trị sốt rét như quinin và chloroquine đều đã có sẵn. Tuy nhiên, sau vài ngày điều trị, các triệu chứng vẫn không hề có dấu hiệu thuyên giảm và sức khỏe, thậm chí là mạng sống của bạn ngày càng bị đe dọa. Khi đó, bạn được thông báo rằng kí sinh trùng sốt rét mình mắc phải là chủng kháng thuốc, có nghĩa là các loại thuốc mà bác sĩ có trong tay đều không thể chữa khỏi bệnh cho bạn (cơ chế của việc kháng chloroquine là do các chủng kháng thuốc phát sinh các đột biến ở các gene Pfmdr1, Pfcg2 và Pfcrt - đây là những gene liên quan đến việc vận chuyển chloroquine vào trong không bào tiêu hóa của trùng sốt rét, khi các phân tử thuốc tích tụ trong không bào tiêu hóa, sẽ làm rối loạn các hoạt động sống của trùng sốt rét và giết chết chúng. Do các gene nêu trên bị đột biến, khả năng hấp thụ chloroquine bị giảm dẫn đến việc trùng sốt rét không bị tác động của thuốc. Còn cơ chế kháng quinine vẫn chưa được hiểu rõ) [8]. Đến lúc này, không những sức khỏe mà cả tâm lý đều ở tình trạng hết sức tệ, tất cả những gì bạn có thể làm là cảm nhận căn bệnh từng ngày hủy hoại cơ thể và sau đó là đe dọa mạng sống của bạn.
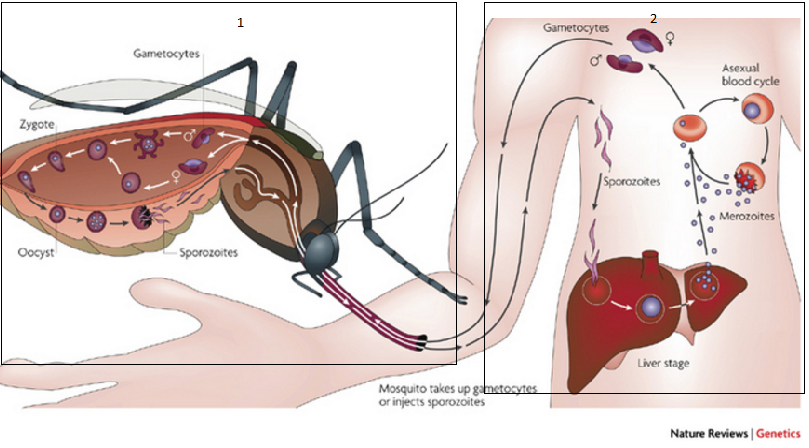
Hình 2: Vòng đời của trùng sốt rét (zygote: hợp tử; oocyst: trứng). Khung số 1 (vòng đời của kí sinh trùng sốt rét trong cơ thể muỗi): muỗi cái Anopheles hút máu người mang mầm bệnh sốt rét đồng thời đưa các giao bào đực và cái của kí sinh trùng vào cơ thể chúng. Các giao bào này kết hợp với nhau tạo thành hợp tử, các hợp tử phát triển thành trứng và sau đó nở thành thoa trùng. Khung số 2 (vòng đời của trùng sốt rét trong cơ thể người): muỗi cái hút máu của một người bình thường đồng thời tạo điều kiện cho các thoa trùng xâm nhập cơ thể nạn nhân, các thoa trùng sau khi vào cơ thể sẽ đến gan, sau đó phát triển thành các mảnh trùng và xâm nhập hồng cầu. Một số mảnh trùng sẽ phát triển thành giao bào đực và cái và chời đến khi có một cá thể muỗi cái khác hút máu người bệnh để xâm nhập cơ thể muỗi và bước vào giai đoạn phát triển trong muỗi. [9]
Đó là những gì mà nhiều nạn nhân sốt rét phải chịu đựng vào những năm 60, 70 thế kỉ trước khi mà các chủng kí sinh trùng sốt rét kháng thuốc dần lan rộng. May mắn cho nhân loại trong cuộc chiến với sốt rét là Đồ U U và nhóm nghiên cứu của bà đã tìm ra được một vũ khí mới vô cùng lợi hại nhờ một chỉ dẫn được để lại từ hàng ngàn năm trước.
2. Tự thuật của nhà khoa học (nội dung phần 2 dựa trên lời kể của chính Đồ U U trong một bài báo [10]):
Tôi bắt đầu sự nghiệp nghiên cứu về các loại thảo mộc ở viện hàn lâm khoa học y dược Trung Quốc sau khi tốt nghiệp đại học y Bắc Kinh năm 1955. Năm 1959, tôi được tham gia một khóa học kéo dài hai năm rưỡi về y học truyền thống Trung Quốc, một khóa học đặc biệt được thiết kế riêng cho những nhà khoa học được đào tạo về y học phương Tây. Đây là cột mốc quan trọng đưa tôi đến với kho báu dược liệu của đất nước đồng thời khai mở cho tôi những hiểu biết, góc nhìn mới về con người và vũ trụ.
Plasmodium falciparum đã là mối họa cho nhân loại suốt hàng ngàn năm. Sau nhiều nỗ lực của cộng đồng quốc tế nhằm loại bỏ căn bệnh này trong thập kỉ 50, sốt rét quay trở lại chủ yếu do sự xuất hiện của các chủng kí sinh trùng kháng các loại thuốc sốt rét vào thời điểm đó, ví dụ như chloroquine. Năm 1967, dự án chống sốt rét cấp quốc gia được triển khai dưới cái tên “dự án 523”. Tôi được chỉ định làm trưởng một nhóm nghiên cứu gồm các nhà dược liệu và dược lí học trẻ tuổi. Nhóm của chúng tôi có nhiệm vụ tách và phân lập các hợp chất có tiềm năng trong các loại thảo mộc Trung Quốc.
Trong giai đoạn đầu, chúng tôi đã phân tích hơn 2000 bài thuốc cổ truyền và nhận thấy 640 mẫu có hoạt tính kháng trùng sốt rét. Giai đoạn sau, chúng tôi tách chiết các hợp chất từ khoảng 200 loại thảo mộc và tiến hành thử nghiệm trên chuột. Quá trình nghiên cứu không hề dễ dàng cũng như không có kết quả đáng kể nào được thu nhận. Bước ngoặt quan trọng trong quá trình nghiên cứu xuất hiện khi dịch chiết của cây Artemisia annua L. (thanh hao hoa vàng, thuộc họ ngải) cho kết quả khả quan trong việc ức chế trùng sốt rét. Tuy nhiên, các lần lặp lại sau đó không cho kết quả mong đợi như thí nghiệm đầu và trái ngược với những ghi chép trong tài liệu cổ mà chúng tôi tìm hiểu trước đó.

Hình 3: a: hình vẽ cây thanh hao hoa vàng trong một tài liệu từ thời nhà Minh; b: cây thanh hao hoa vàng.
Đi tìm lời giải thích cho kết quả trên, chúng tôi xem xét thật kĩ tư liệu mà mình có: “Cẩm nang những bài thuốc cho trường hợp khẩn cấp” của một thầy thuốc thời nhà Tấn, đó là tài liệu duy nhất đề cập đến cách trị sốt rét bằng cây thanh hao hoa vàng. “Ngâm một nắm thanh hao trong hai lít nước, vắt lấy nước cốt và uống hết”, sau khi nghiền ngẫm câu chỉ dẫn trong sách, tôi nảy ra ý tưởng rằng chính nhiệt độ cao trong phương pháp tách chiết (phương pháp tách chiết bằng ethanol) đã làm biến đổi các hợp chất trong cây thuốc, vì vậy sử dụng phương pháp có nhiệt độ thấp hơn (phương pháp tách chiết bằng ether-nhiệt độ tách chiết chỉ vào khoảng 50oC) có thể bảo tồn hoạt tính của dược liệu. Dĩ nhiên sau đó chúng tôi đã thu được dịch chiết có hoạt tính cao hơn rất nhiều. Tiếp theo, tôi và nhóm của mình tiếp tục tách dịch chiết thành hai phần là phần có tính acid (có độc tính và không có hoạt tính chống sốt rét) và phần có tính trung hòa (ít độc tính hơn đồng thời là có hoạt tính mong muốn). Thành quả cuối cùng đến với chúng tôi vào ngày 4 tháng 11 năm 1971 khi hỗn hơp thu được hoàn toàn không có độc tính và hiệu quả diệt trùng sốt rét trên chuột và khỉ là 100%.

Hình 4: a: “Cẩm nang những bài thuốc cho trường hợp khẩn cấp” bản in lại dưới thời nhà Minh; b: câu hướng dẫn cách trị sốt rét bằng thanh hao hoa vàng nằm ở cột thứ năm từ phải sang
Tuy nhiên, thử nghiệm lâm sàng trên người vào thời điểm đó là không thể thực hiện được do những phức tạp của cách mạng văn hóa. Để cứu những bệnh nhân sốt rét, tôi và các đồng nghiệp không còn cách nào khác là trở thành những người đầu tiên thử hỗn hợp vừa thu được. Sau khi đã đảm bảo hợp chất an toàn cho người, chúng tôi đến Hải Nam để chữa cho những bệnh nhân sốt rét nhiễm cả P. vivax và P. falciparum. Kết quả hết sức khả quan: bệnh nhân hồi phục nhanh chóng so với những người được chữa bằng chloroquine.
Vui mừng vì những kết quả thu được, nhóm của tôi tiếp tục nghiên cứu và tìm cách tinh sạch hợp chất có hoạt tính trong hỗn hợp dịch chiết. Một năm sau, chúng tôi đã thu được một sesquiterpene lactone, không màu, nặng khoảng 282 Da (đơn vị đo khối lượng phân tử), công thức phân tử là C15H22O5 và nhiệt độ nóng chảy vào khoảng 156-157oC, chính là hợp chất mang hoạt tính. Chúng tôi đặt tên cho hợp chất là artemisinin.
Joseph Goldstein (nhà sinh hóa học từng đoạt giải Nobel) đã từng nói rằng khám phá và sáng tạo là hai lộ trình trên con đường đến với những phát kiến trong lĩnh vực y sinh. Những gì chúng tôi đã làm được lúc đó chính là bước đầu tiên-sự khám phá, bước tiếp theo chính là sự sáng tạo. Chúng tôi nhận thấy rằng artemisinin có tính tan kém trong nước và dầu cũng như tỉ lệ tái nhiễm của bệnh nhân chữa trị bằng artemisinin là khá cao, vì vậy, các nhà hóa dược của dự án đã có một đóng góp to lớn và vô cùng quan trọng trong cuộc chiến với sốt rét bằng việc nghiên cứu sâu hơn về mối liên hệ giữa cấu trúc hóa học và hoạt tính sinh học của hợp chất cũng như tạo ra các dẫn xuất của artemisinin để cải thiện các khuyết điểm của thuốc. Cuối cùng, dihydroartemisinin (DHA), biến thể có gắn thêm nhóm hydroxyl của arteminisin ra đời, ổn định và có hoạt tính mạnh hơn gấp mười lần so với hợp chất gốc. Quan trọng hơn, tỉ lệ tái nhiễm giảm rõ rệt khi bệnh nhân được chữa trị bằng DHA. Hiệu quả của artemisinin và các biến thể của nó trong việc chữa trị thành công cho hàng ngàn bệnh nhân sốt rét ở Trung Quốc đã thu hút sự chú ý của thế giới trong thập kỉ 80.
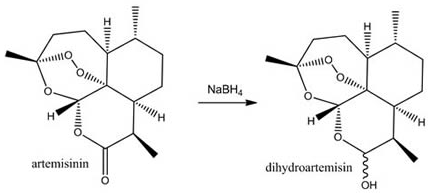
Hình 5: artemisinin và biến thể dihydroartemisinin.
Năm 2005, WHO tuyên bố chuyển đổi chiến lược trong cuộc chiến với sốt rét bằng việc đưa ra “liệu pháp điều trị kết hợp arteminisin” (ACT) (điều trị sốt rét bằng artemisinin/dihydroartemisinin kết hợp với các thuốc không có nguồn gốc artemisinin để tăng hiệu quả điều trị và ngăn khả năng phát sinh chủng kháng thuốc). Đến nay ACT đã được áp dụng rộng rãi trên toàn cầu, cứu sống rất nhiều người, hầu hết là trẻ em ở châu Phi.
3. Cơ chế tác động.
Cho đến nay, cơ chế tác động chính xác của artemisinin đối với kí sinh trùng vẫn chưa được được hiểu rõ hoàn toàn. Hiện tại, có một số giả thiết (đã được chứng minh bằng nhiều thực nghiệm nhưng vẫn còn cần được nghiên cứu chuyên sâu hơn) được giới khoa học tạm thời chấp nhận rộng rãi:
Thứ nhất: như đã nói ở trên, trùng sốt rét ở dạng mảnh trùng sau khi xâm nhập vào hồng cầu sẽ hấp thụ các phân tử hemoglobin (là một đại phân tử được cấu tạo từ 4 tiểu phần, mỗi tiểu phần là một phân tử protein có tên globin, 4 tiểu phần này được chia thành hai nhóm là a globin và b globin, mỗi tiểu phần globin liên kết với một nhóm heme) để sử dụng như nguồn cung cấp chất dinh dưỡng. Nhóm heme (là một phân tử hữu cơ có một nguyên tử sắt ở trung tâm, nguyên tử sắt này có nhiệm vụ liên kết với oxi, từ đó, toàn bộ phân tử hemoglobin trong hồng cầu trở thành những chất mang oxi và hồng cầu đóng vai trò phân phối oxi đi khắp cơ thể) trong phân tử hemoglobin sẽ được giải phóng khi Plasmodium tiêu hóa thức ăn. Đối với kí sinh trùng, nhóm heme là một chất độc và phải được trung hòa thông qua phản ứng polyme hoá (phản ứng liên kết các phân tử nhỏ thành một chuỗi lớn) để tạo thành phân tử heamozoin ít độc. Tuy nhiên, nếu artemisinin xuất hiện trong tế bào trùng sốt rét, các nguyên tử sắt trong nhóm heme sẽ phân cắt cầu nối peroxide (liên kết O-O) trong phân tử artemisinin tạo thành các gốc tự do. Đến lượt mình, các gốc tự do này sẽ alkyl hóa (gắn gốc alkyl) lên phân tử heme và cản trở quá trình polymer hóa heme. Sau một thời gian, heme tích tụ trong tế bào và gây độc cho Plasmodium.
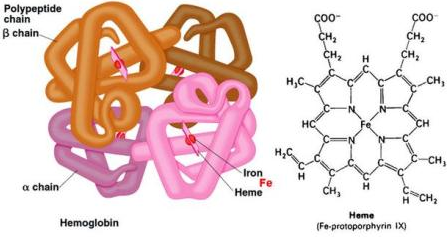
Hình 6: bên trái: cấu trúc hemoglobin gồm 4 tiểu phần globin chia thành 2 nhóm: a globin (màu hồng và tím) và b globin (màu nâu nhạt và nâu sẫm), trong mỗi tiểu phần là một nhóm heme; bên phải: công thức cấu tạo nhóm heme.
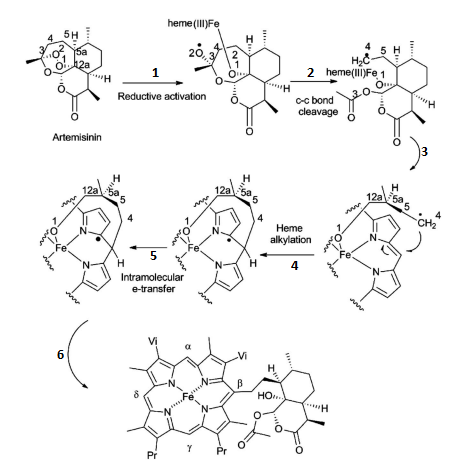
Hình 7: Cơ chế tương tác của artemisinin với nhóm heme: 1: nguyên tử Fe trong nhóm heme hình thành liên kết với O1 của cầu nối peroxide (-O-O-) trong phân tử artemisinin, nguyên tử oxi còn lại của cầu nối peroxide (O2) trở thành một gốc tự do (mang một electron tự do hình thành do sự phá vỡ liên kết O-O); 2: gốc tự do oxi có khả năng hoạt động hóa học mạnh và bẻ gãy liên kết ở carbon ở vị trí số 3 và 4, đến lượt mình, carbon ở vị trí số 4 (C4) trở thành một gốc tự do; 3: gốc tự do ở vị trí carbon số 4 do có khả năng hoạt động hóa học mạnh bắt đầu tấn công cấu trúc của phân tử heme (phá vỡ các liên kết hóa học trong phân tử heme và hình thành liên kết mới); 4: quá trình alkyl hóa heme (hình thành liên kết giữa carbon trên nhóm heme (carbon ở vị trí meso) với carbon của artemisinin (carbon số 4)); 5: electron tự do từ carbon số 4 di chuyển vào bên trong phân tử heme; 6: quá trình hình thành liên kết giữa heme và artemisinin hoàn tất, phân tử heme không thể tham gia vào phản ứng polymer hóa và sẽ tích tụ lại trong tế bào kí sinh trùng sốt rét [11].
Thứ hai: SERCA (sarco-endoplasmic reticulum calcium adenosine triphosphatase) là một enzyme có chức năng duy trì nồng độ ion canxi trong tế bào trùng sốt rét cũng như các loài động vật khác ở mức thích hợp. Ion canxi đóng vai trò trong việc truyền tín hiệu trong tế bào cũng như tham gia vào vào quá trình hoàn thiện các protein. Do sự tương đồng về cấu trúc của artemisinin với thapsigargin (là hợp chất tự nhiên có khả năng ức chế không cạnh tranh đối với SERCA và được trích từ cây Thapsia garganica) nên sự xuất hiện của artemisinin trong tế bào sẽ ngăn cản hoạt động của enzyme trên từ đó làm rối loạn nồng độ ion canxi nội bào và các hoạt động sống của kí sinh trùng. Đến nay, các nhà khoa học đã xác định được ở P. falciparum chỉ có duy nhất một loại SERCA là PfATP6 và các nghiên cứu sâu hơn cũng cho thấy sự tương đồng về cấu trúc của PfATP6 với các loại SERCA của động vật có xương sống là rất thấp (chỉ khoảng 46%) [12] [13] [14], điều đó chứng minh cho việc artemisinin sẽ chỉ tác động chuyên biệt lên enzyme SERCA của trùng sốt rét mà không ảnh hưởng đến bệnh nhân [14].
Thứ ba: Trong tế bào Plasmodium (cũng như các loài sinh vật có nhân hoàn chỉnh khác) tồn tại một loại bào quan gọi là ti thể (mitochondria). Được xem như là nhà máy năng lượng của tế bào, ti thể tạo ra năng lượng nhờ các protein đặc biệt trên màng của bào quan này. Các protein trên màng ti thể hình thành nên một hệ thống phức tạp gọi là chuỗi truyền electron (e): giống như nước đổ từ trên cao xuống dưới thấp làm quay tuốc bin để sinh ra dòng điện, chuỗi truyền e cho các hạt electron mang năng lượng lớn truyền qua, từ đó cung cấp năng lượng cho một enzyme đặc biệt trên chuỗi truyền e tổng hợp nên ATP, nguồn năng lượng chính của hầu hết tế bào sống. Tuy nhiên, nếu có artemisinin trong tế bào, chuỗi truyền e sẽ trở thành nguồn cung cấp electron kích hoạt artemisinin tạo thành các gốc oxi hóa (ROS-reactive oxygen species). Các gốc này sau đó lại tấn công các thành phần khác trong tế bào, phá hủy cấu trúc các phân tử nội bào dẫn đến cái chết cho trùng sốt rét. Các thử nghiệm thực tế trên ti thể của động vật có vú cho thấy không có bất kì tác động nào của artemisinin lên bào quan này ở động vật có vú và ở người. Đến nay, các nhà khoa học vẫn chưa thể giải thích được tại sao artemisinin chỉ phá hủy ti thể của trùng sốt rét (và tế bào nấm men) mà không ảnh hưởng ti thể của người [15] [16].

Hình 8: Sơ đồ chuỗi truyền e và sự tác động của artemisinin lên màng ti thể. I, II, III, IV, Q, C: các phức hợp protein trên màng ti thể, các phức hợp này sẽ tham gia vào các phản ứng oxi hóa-khử trong đó I và II sẽ oxi hóa các hợp chất giàu năng lượng là NADH (Nicotinamide adenine dinucleotide) và succinate làm giải phóng các electron mang năng lượng lớn vào chuỗi truyền electron. Sau đó, các electron này được I và II truyền cho các phức hợp Q rồi đến III, C và cuối cùng là IV. Quá trình vận chuyển electron này sẽ sinh ra năng lượng cung cấp cho hoạt động sống của tế bào. Khi electron được chuyển đến phức hợp IV, chúng sẽ kết hợp với oxi và ion H+ để tạo thành sản phẩm cuối cùng của quá trình là nước. Qua thực nghiệm, các nhà khoa học cho rằng artemisinin (ART) có thể được tác động bởi các electron năng lượng lớn trong chuỗi truyền electron để trở thành những gốc oxi hóa có khả năng hoạt động hóa học mạnh (ROS) (kí hiệu trên hình: ART+). Đến lượt mình, các gốc hoạt động mạnh này sẽ làm rối loạn hoạt động của chuỗi truyền electron và dẫn đến cái chết của kí sinh trùng sốt rét. Cơ chế cụ thể và lí do artemisinin không tác động ti thể của động vật có vú vẫn chưa được hiểu rõ [17].
Ngoài ra, một số thử nghiệm cũng cho thấy có sự tương tác giữa artemisinin với một số protein trong tế bào trùng sốt rét (ví dụ như các protein trên màng tế bào), những tương tác này có thể đóng một vai trò nào đó trong việc tiêu diệt kí sinh trùng [13][15].
4. Vài dòng kết luận:
Giải Nobel dành cho Đồ U U vào năm 2015 là lời nhắc nhở đối với thế giới về sự nguy hiểm tiềm tàng của bệnh truyền nhiễm vì cuộc chiến với kí sinh trùng sẽ không bao giờ chấm dứt khi cứ sau một thời gian những chủng mới có khả năng kháng thuốc sẽ xuất hiện (ví dụ: chloroquine, thuốc trị sốt rét, được phát minh vào năm 1934 và những chủng kí sinh trùng kháng thuốc được ghi nhận vào những năm 50 của thế kỉ trước; melarsoprol, loại thuốc được dùng để đối phó với kí sinh trùng gây bệnh ngủ Trypanosomoa brucei gambiense ở châu Phi, được sử dụng rộng rãi từ năm 1949 nhưng đã ghi nhận sự xuất hiện của chủng kháng thuốc vào cuối thập kỉ 90; bệnh do nhiễm kí sinh trùng thuộc họ Leishmania (Leishmaniasis, căn bệnh gây ra những vết lở loét ở da và tổn thương nội tạng) đã được điều trị bởi Antimonials
từ thập kỉ 50 nhưng sau 30 năm đã xuất hiện chủng kháng thuốc…). Nguyên nhân chính cho sự phát sinh các chủng kháng thuốc đến từ sự sử dụng thuốc diệt kí sinh trùng quá mức: bác sĩ chẩn đoán sai dẫn đến việc sử dụng các loại thuốc không phù hợp, người bệnh tự ý sử dụng kháng sinh khi chưa có hướng dẫn của bác sĩ, lạm dụng thuốc trong chăn nuôi… [18]
Giải thưởng năm đó còn là một sự vinh danh y học cổ truyền: trong cuộc chiến với kí sinh trùng nói riêng và bệnh tật nói chung, loài người có thể giành được phần thắng vì đâu đó ngoài thiên nhiên và trong những trang sách cổ vẫn còn ẩn chứa vô vàn vũ khí kì diệu chờ được khám phá hoặc tái khám phá.
Tài liệu tham khảo:
[1] "Malaria," WHO, [Online]. Available: http://www.who.int/malaria/en/.
[2] "Malaria," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/Malaria.
[3] B. Autino, A. Noris, R. Russo and F. Castelli, "Epidemiology of Malaria in Endemic Areas," Mediterranean Journal of Hematology and Infectious Diseases, vol. 4, no. 1, 2012.
[4] A. Critchlow, J. Staves and C. Watt, "Malaria Vaccines," Stanford university, [Online]. Available: http://web.stanford.edu/class/humbio153/MalariaVac/index.html.
[5] S. Aryal, "Differences Between Plasmodium falciparum and Plasmodium vivax," Online Microbiology Notes, 22 May 2015. [Online]. Available: Online Microbiology Notes.
[6] S. Antinori, L. Galimberti, L. Milazzo and M. Corbellino, "Biology of Human Malaria Plasmodia Including Plasmodium Knowlesi," Mediterranean Journal of Hematology and Infectious Diseases, vol. 4, no. 1, 2012.
[7] "Malaria Fact sheet N°94," WHO, March 2014. [Online]. Available: https://web.archive.org/web/20140903002027/http://www.who.int/mediacentre/factsheets/fs094/en/.
[8] J. Le Bras and R. Durand, "The mechanisms of resistance to antimalarial drugs in Plasmodium falciparum," Fundamental & Clinical Pharmacology, vol. 17, no. 2, pp. 147-153, 2003.
[9] X. Su, K. Hayton and T. E. Wellems, "Genetic linkage and association analyses for trait mapping in Plasmodium falciparum," Nature genetics, vol. 8, pp. 497-506, 2007.
[10] Y. Tu, "The discovery of artemisinin (qinghaosu)," Nature Medicine, vol. 17, pp. 1217-1220, 2011.
[11] N. Yadav, C. Sharma and S. K. Awasthi, "Diversification in the synthesis of antimalarial trioxane and tetraoxane analogs," RSC Advances, vol. 4, p. 5469–5498, 2014.
[12] M. Kimura, Y. Yamaguchi, S. Takada and K. Tanabe, "Cloning of a Ca2 -ATPase gene of Plasmodium falciparum and comparison," Journal of Cell Science, vol. 104, pp. 1129-1136, 1993.
[13] L. Cul, "Discovery, mechanisms of action and combination therapy of artemisinin," Expert Review of Anti-Infective Therapy, vol. 7, no. 8, pp. 999-1013, 2009.
[14] U. Eckstein-Ludwig, R. J. Webb, I. D. A. van Goethem, J. M. East, A. G. Lee, M. Kimura, P. M. O’Neill, P. G. Bray, S. A. Ward and S. Krishna, "Artemisinins target the SERCA of Plasmodium falciparum," Nature, vol. 424, pp. 957-961, 2003.
[15] J. Li and B. Zhou, "Biological Actions of Artemisinin: Insights from Medicinal," Molecules, vol. 15, pp. 1378-1397, 2010.
[16] X. .. Ding, H.-P. Beck and G. Raso, "Plasmodiumsensitivity to artemisinins: magic bullets hit elusive targets," Trends in Parasitology, vol. 27, no. 2, pp. 73-81, 2011.
[17] C. Sun and B. Zhou, "The molecular and cellular action properties of artemisinins: what has yeast told us?," Microbial Cell, vol. 3, no. 5, pp. 196-205, 2016.
[18] A. H. Fairlamb, N. A. Gow, K. R. Matthews and A. P. Waters, "Drug resistance in eukaryotic microorganisms," Nature Microbiology, vol. 1, pp. 1-15, 2016.
[19] "The 2015 Nobel Prize in Physiology or Medicine - Press Release," [Online]. Available: https://www.nobelprize.org/nobel_prizes/medicine/laureates/2015/press.html.
[20] L. H. Miller and X. Su, "Artemisinin: Discovery from the Chinese Herbal Garden," Cell, vol. 146, no. 6, pp. 855-858, 2011.
[21] S. R. Meshnick, "Artemisinin: mechanisms of action, resistance and toxicity," International Journal for Parasitology, vol. 32, p. 1655–1660, 2002.
[22] Y. Li, "Qinghaosu (artemisinin): Chemistry and pharmacology," Acta Pharmacologica Sinica, vol. 33, pp. 1141-1146, 2012.
[23] "List of Plasmodium species," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/List_of_Plasmodium_species.
[24] "Plasmodium falciparum," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/Plasmodium_falciparum#Severe_malaria.
[25] F. T. Aweeka and P. I. German, "Clinical Pharmacology of Artemisinin-Based Combination Therapies," Clinical Pharmacokinetics, vol. 47, no. 2, pp. 91-102, 2008.
[26] X. Su and L. H. Miller, "The discovery of artemisinin and Nobel Prize in Physiology of medicine," Science China. Life Sciences, vol. 58, no. 11, pp. 1175-1179, 2015.
[27] M. A. van Agtmael , T. A. Eggelte and C. J. van Boxtel, "Artemisinin drugs in the treatment of malaria: from medicinal herb to registered medication," Trends in Pharmacological Sciences, vol. 20, no. 5, pp. 199-205, 1999.
[28] J. Wang, L. Huang, J. Li, Q. Fan, Y. Long, Y. Li and B. Zhou, "Artemisinin Directly Targets Malarial Mitochondria through Its Specific Mitochondrial Activation," Plos One, vol. 5, no. 3, pp. 1-12, 2010.
[29] A. F. Cowman and B. S. Crabb, "Invasion of Red Blood Cells by Malaria Parasites," Cell, vol. 124, no. 4, pp. 755-766, 2006.
[30] "P-type ATPase," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/P-type_ATPase.
[31] L. Aravind, L. M. lyer, T. E. Wellems and L. H. Miller, "Plasmodium Biology Genomic Gleanings," Cell, vol. 115, pp. 771-785, 2003.
[32] C. L. Ventola, "The Antibiotic Resistance Crisis," Physical therapy, vol. 40, no. 4,