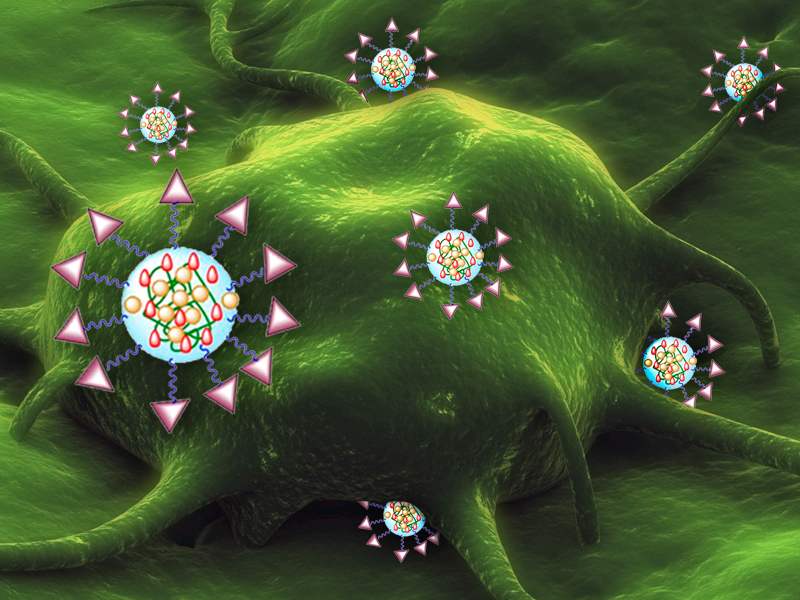
Theo nghiên cứu được công bố vào ngày 28/03/2016 trên Kỷ yếu của Viện Hàn lâm Khoa học Quốc gia Hoa Kỳ, các nhà khoa học đã tạo được loại hạt nano có khả năng thông báo về tình trạng đáp ứng trị liệu của khối u. Việc ứng dụng loại hạt này trong tương lai cho phép các bác sĩ có thể theo dõi hiệu quả điều trị ung thư theo thời gian thực, điều mà các phương pháp điều trị ung thư hiện tại vẫn chưa làm được [1].
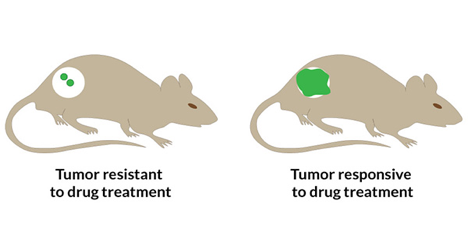
Hình 1: Minh họa sự phát tín hiệu của hạt nano trong khối u kháng (trái) và
khối u nhạy cảm với thuốc (phải). Nguồn: Science News.
Mỗi hạt nano trong nghiên cứu được thiết kế có kích thước khoảng 100 nanomet, gồm ba thành phần: một tác nhân hóa trị hoặc miễn dịch gây độc tế bào đóng vai trò như yếu tố tác động (effector element), một phức hợp chất phát huỳnh quang - chất ức chế đóng vai trò như yếu tố báo cáo thông tin (reporter element) và chúng liên kết với nhau bằng một khung polymer [2].
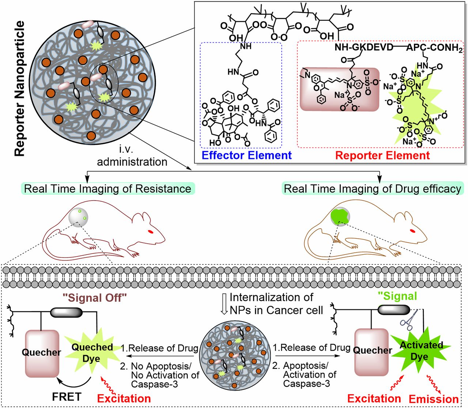
Hình 2: Cấu tạo và cơ chế hoạt động của hạt nano báo cáo thông tin. Nguồn: PNAS.
Khi các thành phần ở trạng thái liên kết nguyên vẹn trong hạt nano, chất phát huỳnh quang bị ức chế nên yếu tố báo cáo thông tin ở trạng thái tắt. Khi các hạt nano này được tiêm vào mạch máu chuột bị ung thư thì sẽ tích tụ tại các tế bào khối u do hiệu ứng EPR(*), và giải phóng yếu tố tác động vào tế bào [2]. Sau đó hai trường hợp có thể xảy ra:
Trường hợp 1: Tế bào khối u nhạy cảm với yếu tố tác động, quá trình chết tế bào (apoptosis) sẽ được khởi động thông qua việc hoạt hóa enzyme caspase-3. Enzyme này không chỉ phá vỡ tế bào khối u thành các mảnh nhỏ mà còn cắt đứt liên kết giữa chất phát huỳnh quang và chất ức chế. Từ đó, yếu tố báo cáo thông tin chuyển sang trạng thái mở, tín hiệu huỳnh quang được phát ra [2].
Trường hợp 2: Tế bào khối u kháng lại yếu tố tác động, enzyme caspase-3 không được kích hoạt, tế bào không chết và yếu tố báo cáo thông tin vẫn ở trạng thái tắt [2].
 Nhóm nghiên cứu đã thử nghiệm hat nano mang paclitaxel, một tác nhân hóa trị gây độc tế bào, trên những con chuột nhắt mang đồng thời hai loại khối u kháng và khối u nhạy cảm với paclitaxel. Kết quả cho thấy khối u nhạy cảm phát ra tín hiệu huỳnh quang có cường độ mạnh gấp khoảng 5 lần so với khối u kháng chỉ 12 giờ sau lần trị liệu đầu tiên [2].
Nhóm nghiên cứu đã thử nghiệm hat nano mang paclitaxel, một tác nhân hóa trị gây độc tế bào, trên những con chuột nhắt mang đồng thời hai loại khối u kháng và khối u nhạy cảm với paclitaxel. Kết quả cho thấy khối u nhạy cảm phát ra tín hiệu huỳnh quang có cường độ mạnh gấp khoảng 5 lần so với khối u kháng chỉ 12 giờ sau lần trị liệu đầu tiên [2].
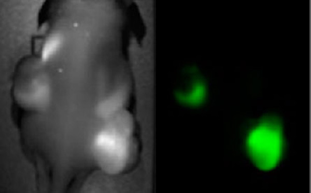
Hình 3: Nửa ngày sau khi được tiêm hạt nano mang paclitaxel, khối u nhạy cảm với thuốc (bên hông phải) tỏa sáng gấp 5 lần khối u kháng (bên hông trái). Nguồn: Science News.
Tiếp đến, tác nhân hóa trị được thay thế bằng kháng thể kháng PD-L1(**). Đây là loại kháng thể có chức năng kích hoạt cơ chế tự phòng vệ của cơ thể chống lại khối u, cho phép các nhà khoa học thử nghiệm hạt nano như tác nhân miễn dịch. Trong thử nghiệm này, các khối u sáng lên một cách đáng kể sau 5 ngày từ khi được trị liệu, qua đó phản ánh độ trễ ban đầu của liệu pháp chữa ung thư bằng miễn dịch so với hóa trị [1, 2].
Nghiên cứu về các hạt nano thông báo tín hiệu đem đến một tiến bộ lớn trong cuộc chiến chống ung thư, bởi hiện nay việc theo dõi tình trạng lâm sàng của khối u được thực hiện thông qua các phép đo gián tiếp hoặc giải phẫu, phải tốn một thời gian dài sau khi tiến hành liệu pháp hóa trị hay miễn dịch để cho ra kết quả. Tuy nhiên, kết quả đó lại có thể không còn phù hợp với tình trạng ung thư hiện tại [2]. Theo Shiladitya Sengupta, đồng tác giả nghiên cứu và là kỹ sư sinh học tại bệnh viện Brigham and Women’s hospital, Boston, thì “đây là hệ thống đầu tiên cho phép bạn đọc thông tin về việc liệu loại thuốc được sử dụng có đang làm việc hay không” [1].
Các bước tiếp theo của nghiên cứu sẽ là thiết kế loại hạt nano sử dụng các vật liệu đã được phê duyệt sử dụng trên lâm sàng và loại thuốc nhuộm có thể theo dõi dễ dàng hơn trong cơ thể người bằng máy MRI(***) [1].
Chú thích:
(*) EPR effect: Enhanced permeability and retention effect (tạm dịch Hiệu ứng thẩm thấu và lưu giữ tăng cường).
(**) PD-L1: Programmed death-ligand 1 (tạm dịch Phối tử 1 kiểm soát sự chết được lập trình – là loại protein xuyên màng thường có ở tế bào khối u gây ức chế hệ thống miễn dịch).
(***) MRI : Magnetic resonance imaging (Chụp cộng hưởng từ).
Tác giả: Nguyễn Minh Khánh (cộng tác viên tạp chí VJS)
Phản biện: Lê Văn Minh (TS, Trung tâm Sâm và Dược liệu Tp. Hồ Chí Minh)
Tài liệu tham khảo
1. Sarah Schwartz (2016), ‘Cancer killers send signal of success’, Science News.
2. Ashish Kulkarni, Poornima Rao, Siva Natarajan, Aaron Goldman, et al. (2016), ‘Reporter nanoparticle that monitors its anticancer efficacy in real time’, PNAS.


