Bài viết nhằm mục đích giới thiệu bệnh lý huyết khối, một trong những bệnh lý có nguy cơ tử vong cao với biến chứng đột quỵ. Đồng thời, tác giả trình bày các nhược điểm của liệu pháp chống đông hiện nay với heparin. Cuối cùng, tóm tắt về một nghiên cứu tổng hợp loại heparin mới, khắc phục được những nhược điểm trên, được gửi tới độc giả.
Bệnh lý huyết khối động tĩnh mạch được định nghĩa là sự xuất hiện các cục máu đông trong động hoặc/và tĩnh mạch, gây tắc nghẽn con đường lưu thông của máu. Huyết khối có thể dẫn đến các vấn đề nguy hiểm như thiếu máu cục bộ tế bào cơ tim, thiếu máu não, thậm chí đột quỵ và tử vong [1]. Có rất nhiều nguyên nhân dẫn đến huyết khối, nhưng cơ bản có ba nguyên nhân chính, còn gọi là tam chứng Virchow (Virchow’s triad): (1) tăng hiện tượng đông cầm máu (hypercoagulability, do di truyền, ung thư, hay bệnh lý miễn dịch), (2) rối loạn tuần hoàn máu (hemodynamic changes, do nằm bất động lâu ngày gây ứ trệ tuần hoàn tĩnh mạch, hoặc do suy tim gây giảm lực chảy động mạch), và (3) tổn thương/bất thường thành mạch (endothelial dysfunction, do viêm nhiễm hay chấn thương) [2,3]. Hiện nay, Trong các phác đồ điều trị huyết khối, các heparin phân tử lượng thấp (low-molecular weight heparins, LMWH, hình 1) được sử dụng rộng rãi như thuốc điều trị [4].Heparin thông thường là loại heparin phân tử lượng cao, được tinh chiết từ động vật như heo, bò. Loại heparin này có nhược điểm là thời gian bán thải dài ngắn và dễ gây tử vong do hội chứng giảm tiểu cầu do heparin (heparin-induced thrombocytopenia, HIT). Do đó, LMWH được ra đời. Tổng hợp từ quá trình chia cắt phân đoạn của heparin thông thường bằng phương pháp hóa học hay sinh học, LMWH khắc phục được những nhược điểm của heparin, có thể tiêm dưới da, và giảm nguy cơ HIT tới tối đa 63% so với heparin thông thường [5,6].
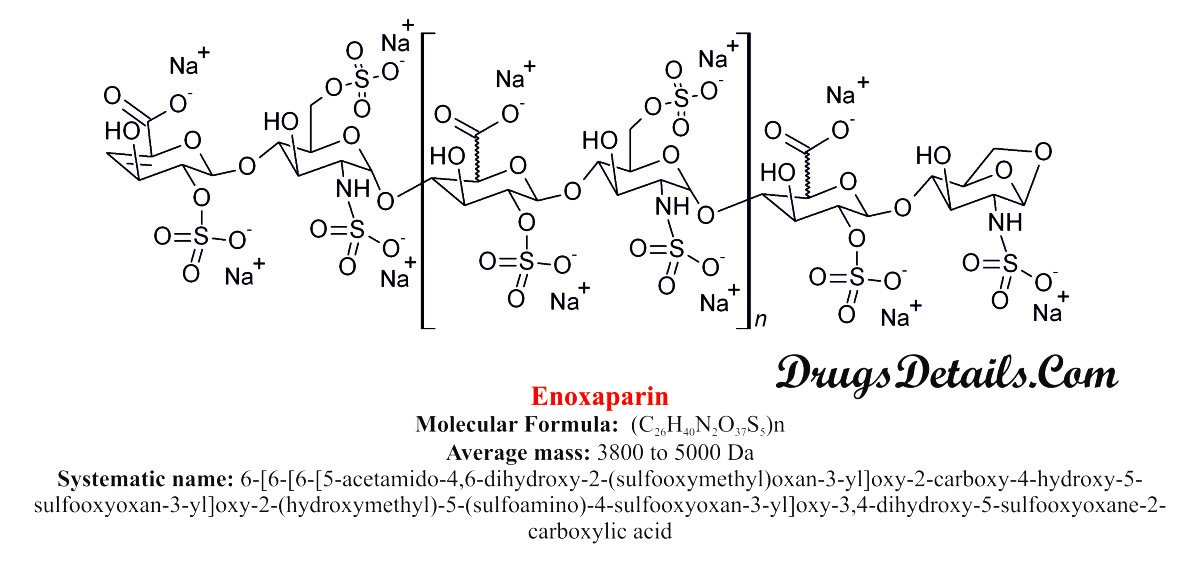
Hình 1: Cấu trúc của heparin phân tử lượng thấp (LMWH), một trong những tên thương mại phổ biến là enoxaparin. Nguồn: DrugsDetails.com
Tuy nhiên, LMWH vẫn còn nhiều nhược điểm, như phải giảm liều trên bệnh nhân suy thận, không thể trung hòa hoàn toàn với protamine trong trường hợp quá liều, và phải dựa vào nguồn cung cấp heparin từ động vật [7]. Việc sử dụng thuốc có nguồn gốc từ động vật từ lâu đã được khuyến cáo là không an toàn do sự bất tương hợp về di truyền của người và động vật, do nguy cơ nhiễm khuẩn cao, do nguồn cung cấp không ổn định cả về mặt số lượng lẫn chất lượng. Insulin trong điều trị đái tháo đường là một ví dụ điển hình. Insulin từ động vật như heo và bò đã dần như biến mất khỏi thị trường, nhường chỗ cho loại insulin tái tổ hợp từ vi khuẩn (như E.coli) [8].
Do đó, nhóm nghiên cứu của Jian Liu và cộng sự đã phát triển một phương pháp hóa sinh mới để tổng hợp LMWH không qua heparin động vật. Kết quả nghiên cứu đã được đăng tải trên tạp chí Science [9]. Phương pháp mới tổng hợp LMWH có 4 bước sau:
1. Tổng hợp 2 loại LMWH: 12-mer-1 và 12-mer-2 (do LMWH có 12 đơn phân đường đơn gắn lại với nhau) bằng con đường hóa sinh học (hình 2).
2. Tinh chế và kiểm tra cấu trúc 2 loại LMWH tổng hợp được bằng các phương pháp phổ học.
3. Đánh giá hiệu quả kháng đông in vitro (trong ống nghiệm) và in vivo (trên chuột) của 2 loại LMWH trên.
4. Kiểm tra độc tính của 2 loại LMWH trên chuột.
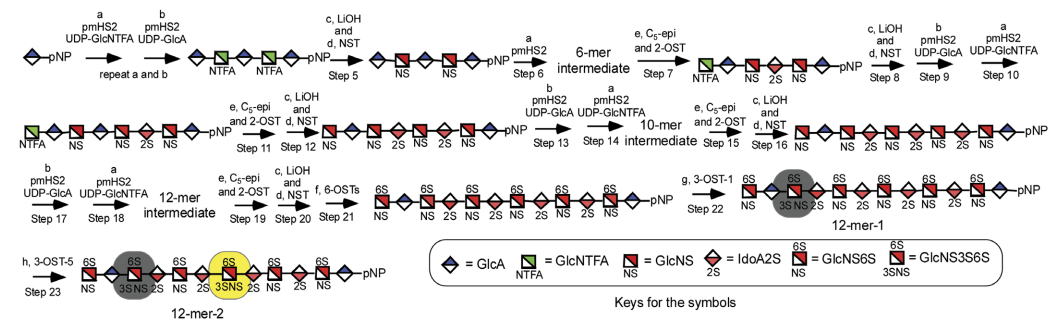
Hình 2: Quy trình hoá sinh học tổng hợp heparin phân tử lượng thấp (LMWH), với 22 bước để tổng hợp 12-mer-1 và 23 bước cho 12-mer-2. Nguồn: [8]
Sau đây xin trình bày chi tiết 4 bước trên:
(1) Quá trình tổng hợp LMWH được tóm tắt trong hình 2. Nguyên liệu ban đầu là phân tử p-nitrophenyl glucuronide (GlcA-pNP) phổ biến trên thị trường, qua hơn 20 bước phản ứng, với việc sử dụng nhiều loại xúc tác hóa học và sinh học (enzym), 2 loại LMWH đã được tổng hợp. Hiệu suất tổng hợp toàn phần cho LMWH-12-mer-1 là 10.3% và LMWH-12-mer-2 là 8.2%.
(2) Các LMWH sau khi tổng hợp được tinh chế và đánh giá độ tinh khiết bằng HPLC (sắc ký lỏng hiệu năng cao, High performance liquid chromatography) với cột trao đổi ion; xác định cấu trúc bằng phổ cộng hưởng từ hạt nhân (Nuclear magnetic resonance, NMR) và khối phổ (Mass spectrometry, MS).
Bước tiếp theo sẽ là đánh giá hoạt tính kháng đông các LMWH tổng hợp này và so sánh với 2 loại heparin khác (Heparin thông thường (heparin động vật, phân tử lượng cao) và enoxaparin – 1 loại LMWH thương mại khác).
(3) Trên yếu tố đông máu Xa, LMWH tổng hợp cho hiệu quả tốt hơn heparin động vật: IC50 khoảng 60 ng/mL so với 110 ng/mL và tương đương enoxaparin. Hơn nữa, LMWH tổng hợp có khả năng bị trung hòa bởi protamine tương đương heparin động vật, gần 100% và cao hơn khoảng 2 lần so với enoxaparin. Điều này có lợi trong trường hợp quá liều LMWH, vì khi đó nhân viên y tế có thể dùng protamine để giải độc. Trên chuột, với liều dùng nhỏ hơn gấp 5 lần, LMWH tổng hợp (liều 1.5 mg/kg) cho tác dụng kháng đông tương đương enoxaparin (liều 7.5 mg/kg). Tuy nhiên, LMWH vẫn cần phải được giảm liều trong trường hợp suy giảm chức năng thận, vì thuốc được đào thải chủ yếu qua thận.
(4) Việc sử dụng LMWH (liều 3600 µg/kg/ngày, gấp khoảng 10 lần liều điều trị, 7 ngày liên tiếp) trên chuột làm giảm bạch cầu, tuy nhiên số lượng tế bào vẫn trong mức cho phép. Đồng thời, chưa tìm thấy độc tính của LMWH trên các chỉ số sinh hóa khác, kể cả trọng lượng các cơ quan quan trọng.
Tóm lại, nhóm nghiên cứu đã thành công trong việc phát triển một phương pháp mới nhằm tổng hợp LMWH một cách lặp lại, an toàn, và khắc phục được một số nhược điểm của LMWH hiện nay. Hy vọng bước tiến này sẽ giúp bệnh nhân có nhiều cơ hội hơn trong việc điều trị bệnh lý huyết khối.
Tác giả: Phạm Duy Toàn – Đại học Naresuan, Thái Lan
Tài liệu tham khảo:
1. Stam J (2005) Thrombosis of the Cerebral Veins and Sinuses. N Engl J Med 352:1791-1798
2. Bagot CN, Arya R (2008) Virchow and his triad: a question of attribution. Br J Haematol 143:180-190.
3. Brotman DJ, Deitcher SR, Lip GYH, Matzdorff AC (2004) Virchow’s Triad Revisited. South Med J 97:213-214.
4. Kahn SR, Lim W, Dunn AS, Cushman M, Dentali F, Akl EA, et al (2012). Prevention of VTE in nonsurgical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 141(2):e195S-e226S.
5. Linhardt RJ, Liu J (2012) Synthetic heparin. Curr Opin Pharmacol 12:217-219.
6. McGowan KE, Makari J, Diamantouros A, Bucci C, Rempel P, Selby R, Geerts W (2016) Reducing the hospital burden of heparin-induced thrombocytopenia: Impact of an avoid-heparin program. Blood 127:1954-1959.
7. Ansell JE, Laulicht BE, Bakhru SH, Hoffman M, Steiner SS, Costin JC (2016) Ciraparatag safely and completely reverses the anticoagulant effects of low molecular weight heparin. Thromb Res 146:113-118.
8. Schernthaner G (1993) Immunogenicity and allergenic potential of animal and human insulins. Diabetes Care 16(3):155-165.
9. Xu Y, Chandarajoti K, Zhang X, Pagadala V, Dou W, Hoppensteadt DM, et al (2017) Synthetic oligosaccharides can replace animal-sourced low–molecular weight heparins. Sci Transl Med 9:eaan5954.


