GHÉP GAN: BÌNH MINH CHO BỆNH GAN GIAI ĐOẠN CUỐI
Tác giả: Nghiên cứu sinh Nguyễn Hải Nam
Khoa Ngoại Gan Mật Tuỵ và Ghép tạng, Đại học Kyoto (Nhật Bản)
Email: nguyenhainam@kuhp.kyoto-u.ac.jp
Bài viết này mong mang lại cho người đọc cái nhìn toàn cảnh cũng như hiểu biết cơ bản về ghép gan một phương pháp điều trị đầy hứa hẹn giúp mở ra hy vọng sống còn cho những bệnh nhân mắc bệnh gan giai đoạn cuối (End staged liver disease, ESLD). Ghép gan là một phương pháp phẫu thuật mới, một thành tựu y học trong thế kỷ 20. Đây là phương pháp chữa trị triệt để duy nhất lúc này cho tình trạng suy gan vì không có máy móc hay thiệt bị nào có thể thay thế các chức năng sống còn của gan với cơ thể. Tại Việt Nam, nếu như trước đây những bệnh nhân xơ gan, những bệnh nhi suy gan giai đoạn cuối do bệnh đường mật bẩm sinh, những em bé một hai tháng tuổi suy gan cấp do bất thường bẩm sinh về chức năng gan,... khắc khoải trông chờ tác dụng của các loại thuốc chỉ giúp hạn chế mức độ tiến triển của bệnh, thì trong những năm ngày đây, với nỗ lực không ngừng của các bác sĩ trong toàn quốc, ghép gan đã mở ra một cuộc đời mới cho họ. Một lá gan mới khỏe mạnh, một tương lai mới tốt đẹp cho bệnh nhân là điều mà chúng tôi, những phẫu thuật viên gan mật tuỵ non trẻ trông chờ, mong mỏi và phấn đấu.
1. Lịch sử, hiện tại và triển vọng tương lai
Năm 1955, tác giả C. Stuart Welch lần đầu tiên mô tả khái niệm ghép gan như một phương pháp điều trị triệt để cho các bệnh nhân mắc bệnh gan giai đoạn cuối. Ba năm sau, tác giả Francis Moore thực hiện ca phẫu thuật ghép gan tự thân đầu tiên ở chó và công bố nghiên cứu của mình trên tạp chí “Transplantation Bulletin” (1). Vào ngày 1 tháng 3 năm 1963, ca phẫu thuật ghép gan đầu tiên trên thế giới ở người được thực hiện tại bệnh viện trường Đại học Colorado bởi phẫu thuật viên người Mỹ Thomas E. Starzl - người được giới y khoa gọi là “cha đẻ của phẫu thuật ghép tạng” (2). Bệnh nhân là một bé trai ba tuổi mắc bệnh hẹp đường mật bẩm sinh được ghép gan như một cứu cánh cuối cùng. Tuy nhiên, bé đã tử vong trong quá trình phẫu thuật vì chảy máu không cầm được do rối loạn đông máu. Theo y văn giai đoạn này ghi nhận, không có trường hợp nào sống quá 23 ngày ở năm ca ghép gan đầu tiên. Nguyên nhân chủ yếu là do tổn thương thiếu máu-tái tưới máu* và tình trạng thải ghép** dẫn đến suy gan và nhiễm trùng. Mặc cho những kết quả hết sức khó khăn vào giai đoạn đầu, bác sĩ Starzl vẫn kiên trì bền bỉ theo đuổi những ca phẫu thuật ghép gan của mình. Năm 1967, một bệnh nhân ghép gan do ung thư gan đã sống được hơn 1 năm và sau đó tử vong do ung thư tái phát. Năm 1989, Starzl công bố 1179 bệnh nhân đã ghép gan thành công với thời gian sống còn sau ghép từ 1 đến 5 năm lần lượt là 73% và 64%, với sự hỗ trợ của các thuốc chống thải ghép như azathioprine và corticoid (3). Và cho đến năm 1990, Tacrolimus – thuốc ức chế miễn dịch thế hệ mới – đã giúp kiểm soát tốt hơn rất nhiều tình trạng thải ghép. Ngày nay, sau hơn 50 năm kể từ ca ghép gan đầu tiên, đã có hơn 20.000 ca ghép gan được thực hiện trên toàn thế giới và tỉ lệ sống còn sau 1 năm đã lên đến 82.1%, sau 5 năm là 67.8% và sau 10 năm là 52.6% (4). Các tình trạng như thải ghép, nhiễm trùng, biến chứng phẫu thuật đã được kiểm soát rất tốt. Quả thật nếu như không có sự kiên định của Starzl bất chấp những kết quả bi quan của những ca phẫu thuật đầu tiên, chúng ta đã không thể có được những thành quả như ngày hôm nay.

Hình 1: “Cha đẻ” của phẫu thuật ghép tạng Thomas E. Starzl (5)
Ngày nay, thành công của phẫu thuật ghép gan cũng như việc giảm dần các chống chỉ định của phương pháp này làm số lượng bệnh nhân chờ ghép ngày một tăng lên, trong khi số lượng người hiến dường như chững lại. Sự bất tương xứng giữa cung và cầu làm tỉ lệ tử vong ở các bệnh nhân chờ ghép tăng lên: thời gian chờ ghép lâu khiến tổng trạng bệnh nhân xấu hơn, cơ hội sống sót hay phục hồi sau ghép giảm dần. Không đầu hàng trước số phận, các nhân viên y tế lại tiếp tục tìm ra các giải pháp mới để làm tăng số lượng gan ghép như: ghép gan phân chia (split liver transplantiation) một gan hiến được ghép cho hai người nhận, sử dụng gan ở người chết não (DDLT: deceased donor liver transplantation, CDLT: cadaveric donor liver transplantation)… nhưng số lượng bệnh nhân chờ ghép cao vẫn là một bài toán nan giải.
Bên cạnh đó, với sự tiến bộ của nền y học hiện đại, các trung tâm ghép gan trên thế giới không ngừng cải thiện kết quả của quy trình ghép gan trên mọi phương diện. Về phương pháp phẫu thuật, nếu như trước đây phẫu thuật lấy gan ở người hiến gan được thực hiện bằng phương pháp mổ mở thì một số trung tâm trên thế giới đã tiên phong trong việc sử dụng phẫu thuật nội soi trong việc lấy gan ghép (6, 7) và gần đây là phẫu thuật robot. Để làm giảm biến chứng mất chức năng của mảnh ghép cũng như giảm tỉ lệ thải ghép* do thời gian thiếu máu mảnh ghép kéo dài, do chất lượng gan ghép không tốt (gan nhiễm mỡ, gan thoái hóa mỡ),… các hệ thống cơ học tái tưới máu** đã ra đời như hệ thống tái tưới máu cơ học hạ thân nhiệt (hypothermic mechanical perfusion) giúp làm giảm quá trình chuyển hóa tế bào ở gan và kéo dài khoảng thời gian tế bào sống sót trong tình trạng thiếu oxygen (8). Ngoài ra, còn có những nghiên cứu đánh giá khả năng giảm liều hoặc ngưng hẳn các thuốc ức chế miễn dịch***, giúp giảm bớt chi phí điều trị và đem lại chất lượng sống tốt hơn cho các bệnh nhân ghép tạng
* thải ghép (transplant rejection) là tình trạng cơ thể không dung nạp với một mô lạ được cấy ghép và cơ thể sẽ tự sản sinh ra các chất làm mô này không tồn tại được và bị thải trừ.
** tổn thương thiếu máu – tái tưới máu (ischemia-reperfusion injury) là tình trạng tổn thương của mô cơ quan xảy ra sau khi nguồn cung cấp máu của mô cơ quan được phục hồi, sau một giai đoạn thiếu máu hay oxy. Bạn đọc có thể hình dung như sau: để ghép gan cho bệnh nhân, gan hiến sẽ được phẫu thuật lấy khỏi cơ thể người hiến và đem ghép cho người nhận, khoảng thời gian từ lúc gan hiến được tách rời khỏi người hiến (cắt các nguồn mạch máu nuôi dưỡng) đến lúc được ghép hoàn toàn vào người nhận nếu kéo dài sẽ làm cho gan hiến bị tổn thương, một số tình trạng không thể hồi phục.
*** ghép gan là đem một mô cơ quan ở cơ thể khác (vật lạ) vào cơ thể người bệnh, khi đó với cơ chế miễn dịch tự nhiên, cơ thể người nhận sẽ sản sinh ra các chất hoá học tấn công vào mảnh gan ghép – quá trình này gọi là thải ghép). Các thuốc ức chế miễn dịch ra đời nhằm mục đích ức chế quá trình này, tạo điều kiện cho mảnh ghép có thể sống và dung hoà trong môi trường cơ thể mới. Tuy nhiên các thuốc này cũng làm giảm đi khả năng miễn dịch của người bệnh, làm người bệnh mất khả năng chống chọi là với các tác nhân vi khuẩn, virus,... cũng như phải chịu đựng các tác dụng phụ của loại thuốc này: đái tháo đường, loãng xương, tiêu chảy, tăng huyết áp...
2. Một số hiểu biết cơ bản về ghép gan
2.1 Cấu trúc và chức năng của gan
Gan là một bộ phận quan trọng của cơ thể. Con người không thể sống nếu như không có gan hoặc mất chức năng gan. Gan giữ nhiều vai trò tích cực như chuyển hóa thuốc và độc chất, loại bỏ các sản phẩm thoái biến của quá trình chuyển hóa bình thường của cơ thể (như loại bỏ ammonia và bilirubin ra khỏi máu) và tổng hợp nhiều protein và enzyme quan trọng như các yếu tố đông máu, các albumin... Gan có 2 nguồn cung cấp máu chính là động mạch gan và tĩnh mạch cửa. Các chất dinh dưỡng và oxygen theo máu đến nuôi dưỡng tế bào gan và tế bào ống mật. Sau đó lượng máu này rời gan theo đường tĩnh mạch gan, đến tĩnh mạch chủ dưới và đổ trực tiếp vào tim. Gan gồm vô số các tế bào gan có tác dụng tạo ra mật và tiết vào các ống mật. Các ống mật li ti đổ vào 2 nhánh mật lớn gọi là ống gan phải và ống gan trái, sau đó đổ vào ống mật chủ và từ đó dịch mật được bài tiết vào ruột. Mật có tác dụng hoà tan các chất béo và tiêu hủy các tạp chất và độc chất từ quá trình chuyển hóa.
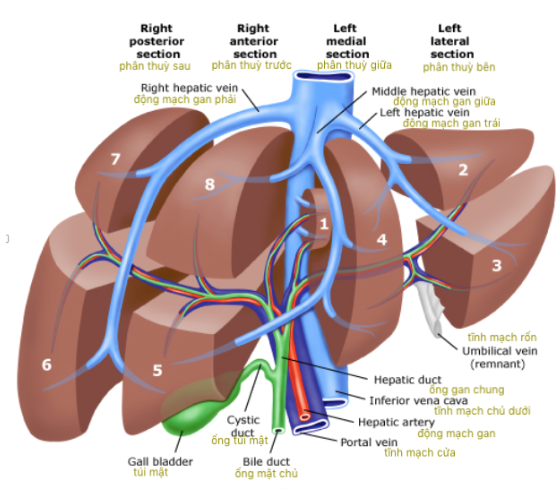
Hình 2: Giải phẫu các cấu trúc của gan (9)
2.2 Các nguyên nhân dẫn đến bệnh gan giai đoạn cuối
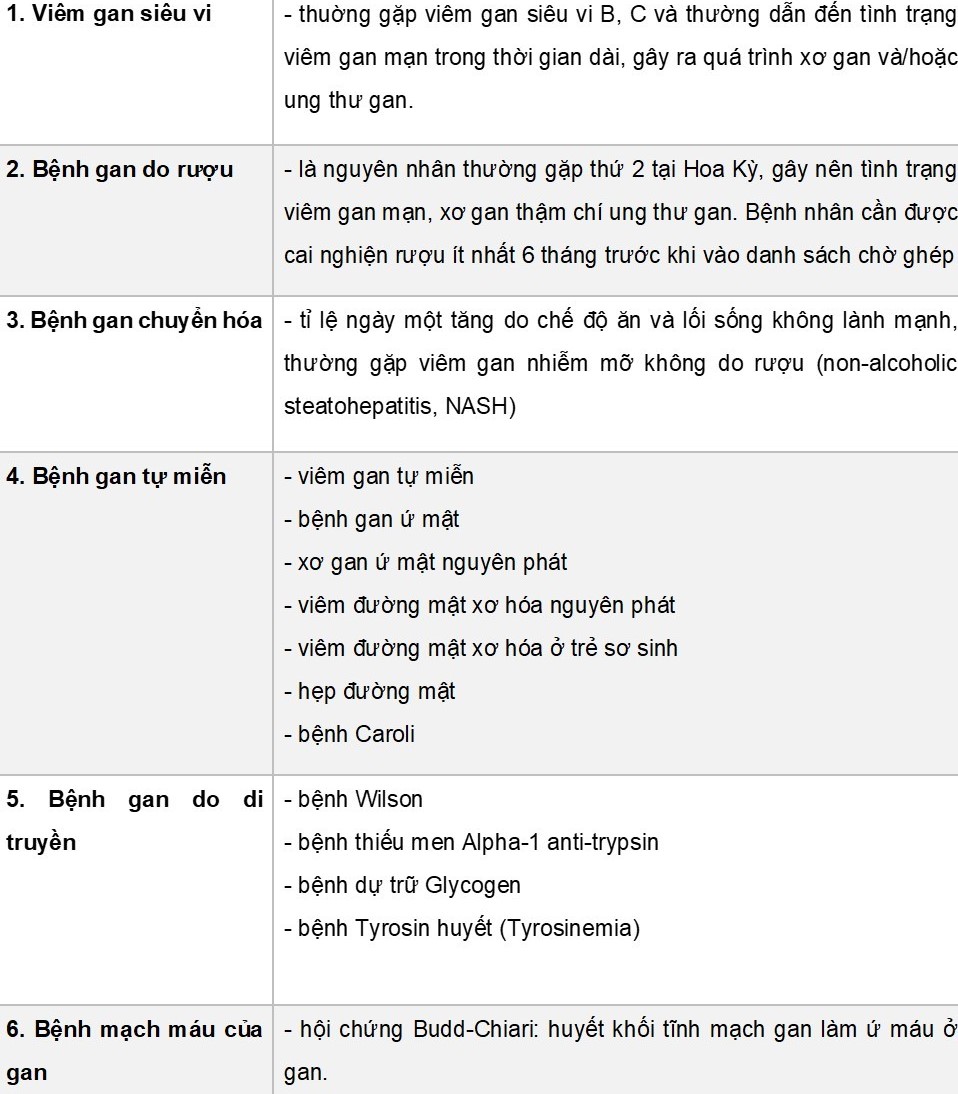
2.3.1. Ghép gan từ người cho chết não (Donation after brain death - DBD liver transplantation)2.3 Phân loại phẫu thuật trong ghép gan
Tình trạng chết não thường xảy ra sau một cơn đột quỵ hoặc chấn thương đầu nặng làm ngưng hoàn toàn các hoạt động của não bộ trong khi các cơ quan khác bao gồm cả gan vẫn hoạt động bình thường. Các tiêu chuẩn để chẩn đoán chết não rất nghiệm ngặt dựa trên sự thiếu vắng hoàn toàn các chức năng của não bộ thông qua các xét nghiệm. Ghép gan từ người cho chết não cần phải được sự đồng ý và cho phép từ người thân trong gia đình của bệnh nhân.
2.3.2. Ghép gan từ người cho ngưng tim (Donation after cardiac death - DCD liver transplantation)
Trong một số trường hợp bệnh nhân có chấn thương đầu mức độ nặng kèm theo tiên lượng không thể phục hồi về mặt thần kinh (chúng ta có thể hiểu là sống thực vật), gia đình của bệnh nhân có thể quyết định ngừng các thiết bị hỗ trợ sự sống cho bệnh nhân để bệnh nhân được chết. Khi đó, cái chết của bệnh nhân không được gọi là chết não mà là ngưng tim. Tạng được phẫu thuật lấy ra trong trường hợp ngưng tim này, trái ngược với tình trạng chết não, có nguy cơ bị thương tổn nhiều hơn trong 2 giai đoạn sau. Giai đoạn đầu là khoảng thời gian từ lúc ngừng các thiết bị hỗ trợ sự sống cho đến lúc người cho mất: các cơ quan trong cơ thể người cho bao gồm cả gan bắt đầu chịu đựng tình trạng thiếu oxygen do hệ thống hô hấp và tuần hoàn bắt đầu ngừng hoạt động. Giai đoạn thứ hai là từ lúc bệnh nhân mất cho đến khi cơ quan hiến tặng được rửa sạch và ngâm trong dung dịch bảo quản và giữ lạnh. Chính vì vậy mà ghép gan từ người cho ngưng tim thường đi kèm với nguy cơ mất chức năng của mảnh ghép, huyết khối động mạch gan và các biến chứng về đường mật.
2.3.3. Ghép gan từ người cho sống (Living donor liver transplantation - LDLT)
Mặc dù mỗi người chỉ có một lá gan và không thể sống nếu không có gan, nhưng gan là cơ quan kì diệu vì nó có thể tái sinh lại một phần sau khi được cắt bỏ. Chính vì vậy mà chúng ta có thể dành một phần lá gan của mình để ghép cho các bệnh nhân khác. Có nhiều cách phân chia gan, mà cách thông thường như hình mô tả dưới đây, giúp các phẫu thuật viên lựa chọn mảnh ghép nào là phù hợp cho người nhận. Tuỳ vào độ tuổi, cân nặng, bệnh lý và các xét nghiệm liên quan của người nhận và cả người cho mà gan sẽ được cắt bên phải, bên trái, hay một thuỳ nhỏ (ghép gan cho trẻ em)... để đảm bảo phần gan ở người nhận và cả người cho sẽ hoạt động bình thường.
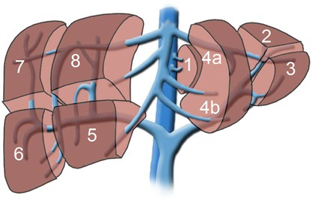
Hình 3: Gan được phân chia chủ yếu thành 8 phân thuỳ (10)
3. Các bước tổng quan trong một quy trình ghép gan
Trong trường hợp ghép gan ở người cho sống, bệnh nhân và người hiến gan sẽ được nhập viện để làm các xét nghiệm và chẩn đoán hình ảnh liên quan. Với người cho, một loạt các đánh giá được thực hiện để xem “Người cho có thể hiến tặng bao nhiêu phần trăm thể tích gan mà vẫn giữ vững hoạt động chức năng sinh lý bình thường của cơ thể?”. Sự an toàn và chất lượng cuộc sống ổn định sau ghép là điều kiện tiên quyết ở người cho. Với người nhận, người ta sẽ cân nhắc xem việc ghép gan có mang lại hiệu quả tích cực trên tổng thể hay không. Ở một số trường hợp như tình trạng bệnh quá nặng, ở giai đoạn suy đa cơ quan, ung thư gan giai đoạn muộn, mắc thêm các bệnh khác không phù hợp cho phẫu thuật… thì ghép gan không mang lại nhiều lợi ích mà nhiều khi chỉ làm tăng tỉ lệ tử vong và rút ngắn thời gian sống của người bệnh. Để chuẩn hóa và đồng bộ hóa, cũng như vì số lượng người hiến gan còn quá ít so với số lượng bệnh nhân chờ ghép, mỗi trung tâm y tế, mỗi quốc gia sẽ có tiêu chuẩn riêng về việc bệnh nhân có đủ điều kiện để được ghép gan hay không và thứ tự ưu tiên dựa trên mức độ nghiêm trọng hiện tại của bệnh nhân. Thang điểm MELD (The Model for End Stage Liveer Disease) được sử dụng để đánh giá và phân loại các trường hợp cần ghép gan không phải cấp tính. Tiêu chuẩn Milan dùng để chỉ định ghép gan ở các bệnh nhân ung thư tế bào gan nguyên phát.
Về phương diện phẫu thuật, thông thường trong trường hợp ghép gan ở người cho sống sẽ có hai bàn mổ được tiến hành song song. Ở người cho, phẫu thuật viên sẽ thực hiện quá trình cắt một phần gan đã tính toán từ trước. Sau đó phần gan này sẽ được chuyển đến một bàn mổ nhỏ trong cùng phòng (back table) và được phẫu thuật viên bơm rửa với dung dịch bảo quản, giữ lạnh cũng như tiến hành đọ đạc kích thước, cân nặng của mảnh ghép và các mạch máu, đường mật và cuối cùng là tạo hình mảnh ghép sao cho phù hợp với cơ thể người nhận. Ở người nhận, phẫu thuật đầu tiên bao gồm việc cắt bỏ hoàn toàn phần gan bệnh lý trước đó ra khỏi cơ thể. Việc cắt bỏ các mạch máu – bước cuối cùng để ngưng sự hoạt động của gan – được thực hiện ngay sau khi phòng mổ bên cạnh thông báo đã hoàn thành bước tạo hình cuối cùng của mảnh ghép. Sau đó mảnh ghép được đặt vào ổ bụng người nhận, tĩnh mạch chủ dưới là mạch máu đầu tiên được khâu nối tiếp theo sau là tĩnh mạch cửa. Kế đến là phục hồi sự lưu thông của động mạch gan bằng cách nối phần động mạch của gan cho vào động mạch của người nhận. Cuối cùng, ống mật chính của gan cho được nối vào đường mật của người nhận sao cho dịch mật từ gan cho bài tiết ra có thể lưu thông vào đường ruột của người nhận.
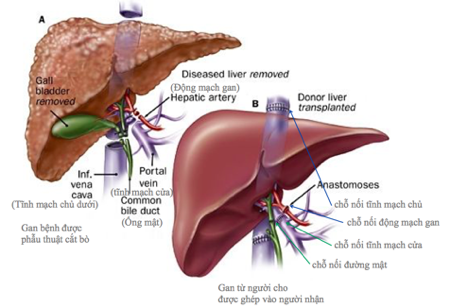
Hình 4: Hình ảnh minh hoạ quá trình ghép các bộ phận của gan (11)
4. Các vấn đề phát sinh sau ghép gan
4.1. Biến chứng phẫu thuật
Bất kì một phương pháp phẫu thuật nào cũng tiềm ẩn những tai biến, biến chứng. Nhiệm vụ của người phẫu thuật viên là phải nắm vững các biến chứng có thể xảy ra và làm giảm nguy cơ xảy ra. Các biến chứng thường gặp ở bệnh nhân ghép gan bao gồm:
- Gan ghép mất chức năng hoặc kém chức năng: tỉ lệ khoảng 1-5%, một số trường hợp cần phải ghép gan lần 2 để cứu bệnh nhân
- Huyết khối, thuyên tắc xuất hiện ở động mạch gan hoặc tĩnh mạch cửa
- Rò mật hoặc hẹp đường mật
- Chảy máu sau mổ
- Nhiễm trùng sau mổ
4.2. Sử dụng thuốc ức chế miễn dịch
Cơ thể người bệnh sẽ nhận biết gan từ người cho – mảnh ghép – là một vật lạ và kích hoạt cơ chế bảo vệ cơ thể qua các phản ứng miễn dịch nhằm chống lại mảnh ghép. Đây cũng là nguyên nhân dẫn đến tình trạng thải ghép. Chính vì vậy, việc sử dụng các thuốc ức chế miễn dịch với mục đích làm suy yếu hệ thống miễn dịch của người bệnh, giúp cho mảnh ghép “sống sót” trong môi trường mới là cần thiết. Các thuốc sau đây thường được phối hợp sử dụng: corticoids, nhóm ức chế calcineurin (cyclosporine, tacrolimus), mycophenolate mofetil, nhóm ức chế mTOR (sirolimus, everolimus), nhóm thuốc basiliximab, daclizumab, nhóm diệt tế bào T khỏi hệ tuần hoàn (thymoglobulin, OKT3). Ở các trung tâm lớn trên thế giới, bên cạnh đội ngũ phẫu thuật viên, mỗi một trường hợp ghép gan sẽ được hội chẩn bởi các chuyên gia miễn dịch chuyên về ghép tạng để đánh giá và đưa ra một phác đồ phù hợp cho mỗi bệnh nhân.
4.3. Vấn đề thải ghép
Thải ghép là tình trạng chức năng của gan mới ghép bị tổn thương và mất chức năng do tác động của hệ miễn dịch ở người nhận. Khi nghi ngờ thải ghép, sinh thiết gan là tiêu chuẩn vàng để chẩn đoán xác định. Thải ghép cấp (acute cellular rejection) xảy ra ở khoảng 25-50% các trường hợp trong năm đầu tiên sau ghép với giai đoạn đỉnh cao là 4-6 tuần đầu sau ghép. Thải ghép mạn (chronic rejection) chiếm tỉ lệ ít hơn, khoảng 5%, với yếu tố nguy cơ là sự lặp đi lặp lại của các đợt thải ghép cấp (13). Vai trò và kinh nghiệm của bác sĩ giải phẫu bệnh là hết sức cần thiết trong giai đoạn này để đánh giá đầy đủ và chính xác tình trạng hiện tại của mảnh ghép.
4.4. Sự tái phát của bệnh gan trước đó
Ngày nay chúng ta đã có nhiều loại thuốc và các phác đồ điều trị nhằm ngăn ngừa tình trạng tái nhiễm ở mảnh ghép gan mới với kết quả khá thuyết phục ở bệnh nhân mắc viêm gan siêu vi B. Tuy nhiên, vấn đề tái nhiễm ở bệnh nhân viêm gan siêu vi C vẫn còn nan giải. Những bệnh nhân mang virus viêm gan siêu vi C trong máu sẽ tiếp tục nhiễm virus này sau ghép gan. Trái với việc tái nhiễm viêm gan siêu B thường làm suy gan diễn ra nhanh chóng, việc tái nhiễm viêm gan siêu vi C ảnh hưởng đến chức năng gan chậm hơn và chỉ khoảng 5% bệnh nhân diễn tiến đến xơ gan và bệnh gan giai đoạn cuối trong vòng 2 năm sau ghép gan. Ở các bệnh lý khác, tỉ lệ tái phát viêm đường mật xơ hóa nguyên phát (Primary sclerosing cholangitis, PSC) và xơ gan ứ mật nguyên phát (Primary biliary cirrhosis, PBC) là 10-20% và rất hiếm diễn tiến đến xơ gan và bệnh gan giai đoạn cuối. Các bệnh nhân ung thư gan được phẫu thuật ghép gan vẫn tiềm ẩn nguy cơ tái phát ung thư gan trên nền gan ghép, do đó người bệnh cần tuân thủ chặt chẽ phác đồ theo dõi để đạt được kết quả tốt nhất.
4.5. Nhiễm trùng cơ hội và ung thư
Như đã trình bày, vai trò chính yếu của hệ thống miễn dịch là xác định và tấn công các tác nhân ngoại lai xâm nhập vào cơ thể. Như vậy, đích nhắm của hệ miễn dịch không phải là các cơ quan ghép mà là vi khuẩn, virus, nấm và các vi sinh vật khác. Chính vì vậy, việc sử dụng thuốc ức chế miễn dịch sau ghép gan không những tạo điều kiện thuận lợi cho các bệnh nhiễm trùng, mà còn cả các “nhiễm trùng cơ hội” là các bệnh nhiễm trùng chỉ gặp ở người suy giảm miễn dịch (bệnh nhân AIDS, bệnh nhân lupus…). Hệ miễn dịch cũng có chức năng chiến đấu loại trừ các tế bào ung thư, nên bệnh nhân sau ghép gan, dùng thuốc ức chế miễn dịch sẽ có nguy cơ mắc một số loại ung thư cao hơn người thường.
4.5.1. Rối loạn tăng sinh lympho sau ghép (Post transplant lymphoprolipherative disorder)
Rối loạn tăng sinh lympho sau ghép là một dạng ung thư hiếm gặp, xảy ra ở các bệnh nhân sau ghép. Tác nhân gây bệnh là Epstein-Barr virus (EBV). Phần lớn người trưởng thành đều đã từng tiếp xúc với EBV trong thời thơ ấu hoặc giai đoạn thanh thiếu thiếu niên nhưng không có biểu hiện vì hệ miễn dịch đủ sức để ức chế chúng. Tuy nhiên, ở các bệnh nhân sau ghép có sử dụng thuốc ức chế miễn dịch, EBV tái hoạt động trở lại và gây nên tình trạng trên. Ngày nay với sự phát triển không ngừng của khoa học sức khỏe, rituximab và các loại thuốc có thể giúp kiểm soát được tình trạng trên.
4.5.2. Ung thư da không melanoma (Non-melanoma skin cancer NMSC)
Ung thư da là tổn thương ác tính thường gặp nhất ở bệnh nhân sau ghép tạng với tỉ lệ là 27% sau 10 năm. Chính vì vậy mà nhiều khuyến cáo khuyên các bệnh nhân sau ghép hạn chế tối đa việc tiếp xúc với ánh sáng mặt trời và phải thường xuyên đi kiểm tra da.
Hành trình mà phẫu thuật ghép gan ra đời, phát triển và tồn tại cho đến ngày nay đã trải qua rất nhiều chông gai. Không những thế, quy trình ghép gan từ lúc bệnh nhân nhập viện cho đến lúc nhận định mảnh ghép có thể sống được yên bình trong cơ thể mới cũng hết sức phức tạp, gian truân và nhiều thử thách. Tác giả một lần nữa xin phép được nhấn mạnh rằng ghép gan không chỉ đơn thuần là một phương pháp phẫu thuật mà đó là sự phối hợp của tập thể các chuyên gia y tế thuộc nhiều chuyên ngành: phẫu thuật, gây mê hồi sức, miễn dịch, giải phẫu bệnh... Thành công của một trường hợp ghép gan là công sức của một tập thể làm việc kiên trì và gắn kết. Tác giả mong rằng trong tương lai gần, thành tựu về ghép gan ở Việt Nam sẽ ngày càng vươn xa để các bệnh nhân mắc bệnh gan giai đoạn cuối có thêm cơ hội sống một cuộc đời mới. Qua bài viết, tác giả cũng mong muốn tuyên truyền và cổ xuý cho một hành động nhân đạo và hết sức cần thiết trong thời đại ngày nay: HIẾN TẠNG. “Một cá nhân mất đi nhưng có thể mang lại sự sống cho nhiều người khác”, tác giả tin rằng bất cứ lúc nào chúng ta cũng có thể mang lại sự hữu ích của mình cho cuộc đời này.
TÀI LIỆU THAM KHẢO
1. Meirelles Junior RF, Salvalaggio P, Rezende MB, Evangelista AS, Guardia BD, Matielo CE, et al. Liver transplantation: history, outcomes and perspectives. Einstein (Sao Paulo, Brazil). 2015;13(1):149-52.
2. Arulraj R, Neuberger J. Chapter 97A - Liver transplantation: Indications and general considerations. In: Jarnagin WR, Blumgart LH, editors. Blumgart's Surgery of the Liver, Pancreas and Biliary Tract (Fifth Edition). Philadelphia: W.B. Saunders; 2012. p. 1662-73.e2.
3. Starzl TE, Todo S, Tzakis AG, Gordon RD, Makowka L, Stieber A, et al. Liver transplantation: an unfinished product. Transplantation proceedings. 1989;21(1 Pt 2):2197-200.
4. Waki K. UNOS Liver Registry: ten year survivals. Clinical transplants. 2006:29-39.
5. Kreps G MJ. Thomas E. Starzl, MD, PhD, ‘Father of Transplantation,’ Dies at 90. 2017 [cited; Available from: Available at: http://www.news.pitt.edu/news/thomas-e-starzl-md-phd-father-transplantation-dies-90.
6. Strong RW, Lynch SV, Ong TH, Matsunami H, Koido Y, Balderson GA. Successful liver transplantation from a living donor to her son. The New England journal of medicine. 1990;322(21):1505-7.
7. Raia S, Nery JR, Mies S. Liver transplantation from live donors. Lancet (London, England). 1989;2(8661):497.
8. Weeder PD, van Rijn R, Porte RJ. Machine perfusion in liver transplantation as a tool to prevent non-anastomotic biliary strictures: Rationale, current evidence and future directions. Journal of hepatology. 2015;63(1):265-75.
9. Liver segemental anatomy. [cited; Available from: http://www.aboutcancer.com/liver_mets_anatomy.htm
10. Transplant. IpcoRCoSoIRuCCL. [cited; Available from: http://www.healcentral.org/.
11. Basics LT. [cited; Available from: https://www.pinterest.com/pin/174796029262629683/.


