Trần Thanh Long
Phòng thí nghiệm công nghệ sinh học phân tử, khoa Sinh học – Công nghệ sinh học, trường đại học khoa học Tự Nhiên Tp HCM
Theo ước đoán của các nhà khảo cổ, con người đã biết tạo ra và sử dụng rộng rãi lửa từ cách đây 125 nghìn năm. Lửa mang đến ánh sáng và nhiệt độ, làm thay đổi hoàn sự phát triển của nhân loại cho đến tận ngày nay. [1]
Ngày 22 tháng 11 năm 1879, Thomas Edison, một trong những nhà phát minh vĩ đại của thế giới, đã thành công trong việc tạo ra bóng đèn đầu tiên (sau hơn 1000 lần thất bại). Bóng đèn từ đó tạo nên những tác động to lớn đến cách chúng ta sống, làm việc, giải trí và là tiền đề cho rất nhiều những phát minh lớn nhỏ về sau. Xã hội loài người đã tiến thêm nhiều bước tiến to lớn kể từ khi bóng đèn ra đời. [2]
Một khám phá khác cũng mang những tác động to lớn đến sự phát triển của các ngành khoa học sự sống, mà như viện hàn lâm khoa học hoàng gia Thụy Điển gọi là “ngôi sao soi đường cho lĩnh vực hóa sinh” [3], đã được vinh danh vào năm 2008 bằng giải Nobel hóa học. Đối với nhiều nhà nghiên cứu trong lĩnh vực khoa học sự sống, công trình được trao giải năm đó giống như việc tìm ra lửa hay phát minh ra bóng đèn đối với sự phát triển của xã hội loài người. Tuy nhiên, điều bất ngờ là một công trình có tác động lớn lao như vậy lại bắt nguồn từ một trong những loài động vật đơn giản nhất trong tự nhiên.
Câu chuyện bắt đầu vào giữa trưa ngày 9 tháng 8 năm 1945, cậu bé mười sáu tuổi Osamu Shimomura, lúc này đang làm việc cho một nhà máy cách thành phố Nagasaki 15 km về hướng đông bắc thì nghe thấy tiếng còi báo động một cuộc oanh tạc của quân Đồng Minh sắp diễn ra. Đã quá quen thuộc với tình huống này, thay vì đến hầm trú ẩn, cậu và một vài người bạn trèo lên ngọn đồi gần đó để quan sát cuộc oanh tạc sắp đến. Chỉ có điều, chiếc máy bay B-29 ngày hôm ấy không mang theo những quả bom thông thường mà người dân Nhật Bản đã quá quen thuộc trong suốt cuộc chiến, thứ mà nó sắp thả xuống Nagasaki, cũng giống như thứ đã được thả xuống Hiroshima ba ngày trước, là một loại vũ khí hoàn toàn mới vừa được phát minh và sử dụng lần thứ hai, và cũng hi vọng là lần cuối cùng. Thứ vũ khí mà sau này Osamu mới biết là bom nguyên tử đã hủy diệt gần như toàn bộ Nagasaki. Bị mù tạm thời, chấn động bởi sóng xung kích cũng như bị phơi nhiễm với cơn mưa phóng xạ sau vụ nổ, may mắn với cậu bé và nền khoa học thế giới sau này là cậu vẫn sống sót. [4]
Trong cảnh hỗn loạn sau chiến tranh và vụ nổ bom, Osamu gần như không tìm được nơi nào để bắt đầu việc học đại học. Cuối cùng, lựa chọn duy nhất mà cậu có là nhập học đại học dược Nagasaki. Đối với Osamu, đây chính là quyết định thay đổi cuộc đời cậu mặc dù lúc đó, Osamu không có bất kì hứng thú gì với ngành dược. Osamu sau đó hoàn thành chương trình đại học và làm việc tại phòng thí nghiệm hóa phân tích của trường. Quá trình làm việc chăm chỉ và ấn tượng tại đây đã giúp Osamu được giới thiệu đến làm việc tại phòng thí nghiệm của giáo sư Yoshimasa Hirata, một chuyên gia về hóa hữu cơ, ở đại học Nagoya. Giáo sư Hirata chính là người đã đưa Osamu đến với niềm đam mê lớn nhất của cuộc đời ông, nghiên cứu về sự phát quang sinh học. [4]
Nhiệm vụ đầu tiên của Osamu ở nơi làm việc mới lại là một thách thức không hề nhỏ: thu nhận và tinh sạch vargulin từ Cypridina, một loại giáp sát nhỏ ở vùng biển nông Nhật Bản. Sinh vật này có khả năng phát ra ánh sáng xanh lam (bước sóng 462 nm) thông qua phản ứng oxi hóa một phân tử hữu cơ kích thước nhỏ là vargulin (viết tắt từ chữ vargula luciferin) bằng enzyme vargula luciferase (nhiều phản ứng phát quang sinh học trong tự nhiên diễn ra do phản ứng oxi hóa các hợp chất hữu cơ nhỏ dưới xúc tác của các enzyme đặc biệt. Các hợp chất hữu cơ đó được gọi chung là luciferin và các enzyme xúc tác được gọi là luciferase). Trước đó, nhà khoa học người Mĩ Newton Harvey ở đại học Princeton đã cố gắng tinh chế vargula trong 20 năm nhưng đều thất bại do vargulin cực kì thiếu ổn định và bị phân hủy nhanh chóng nếu tiếp xúc với oxi. Sau 10 tháng làm việc cật lực với rất nhiều lần thất bại, cuối cùng, Osamu cũng tìm ra cách tinh sạch và tinh thể hóa vargulin, từ đó xác định cấu trúc hóa học của hợp chất. Đây là công trình lớn đầu tiên của ông và cũng là tiền đề cho công trình đoạt giải Nobel sau này. [4]
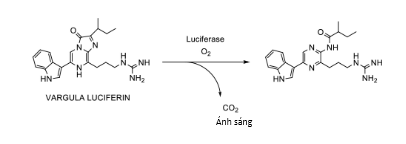
Hình 1: Cấu trúc vargulin và phản ứng phát huỳnh quang của vargulin xúc tác bởi enzyme luciferase. [5]
Với thành công trên, Osamu được mời đến Mĩ và nghiên cứu ở phòng thí nghiệm ở đại học Princeton vào năm 1960, tại đây, ông tiến hành công trình lớn nhất đời mình. Khi vừa đến Princeton, ông được giới thiệu một loại sinh vật nhỏ bé là sứa Aequorea victoria (hay còn có tên gọi khác là Aequorea aequorea), điều thu hút Osamu là khả năng phát quang sinh học với ánh sáng xanh lục của loài sứa này. Sau đó một năm, ông quyết định bắt tay nghiên cứu khả năng phát sáng của sứa A. victoria. Ngày nay, với sự phát triển vũ bão của lí thuyết cũng như kĩ thuật về sinh học phân tử, tin sinh học,… việc nghiên cứu các hợp chất sinh học mới đã trở nên nhanh chóng và đơn giản hơn, tuy nhiên, vào những năm đầu thập kỉ 60, cách duy nhất để các nhà khoa học như Osamu có thể nghiên cứu hợp chất mong muốn là thu thập một lượng mẫu đủ lớn từ tự nhiên. Vì vậy, trong suốt 19 năm, Osamu cùng gia đình và các đồng nghiệp đều đến cảng Friday ở Washington vào mỗi mùa hè để thu mẫu hoàn toàn thủ công chỉ với vợt và lưới. Số lượng sứa được ước lượng dựa trên khối lượng đánh bắt được. Vậy Osamu đã thu tổng cộng bao nhiêu cá thể sứa? Theo chính lời kể của ông, tổng số mẫu thu nhận và xử lí trong suốt thời gian trên là khoảng 850 000! Đúng như Osamu nhận xét: “Đó là nghiên cứu hóa sinh cổ điển”. [4] [6]
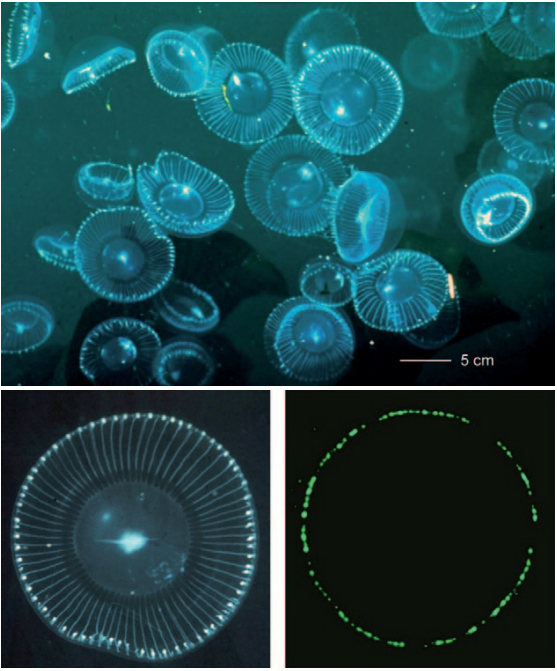
Hình 2: Hình trên: sứa A. victoria trong tự nhiên; hình dưới bên trái: một cá thể sứa nhìn từ phía trên trong điều kiện ánh sáng bình thường; hình dưới bên phải: cá thể sứa phát huỳnh quang xanh lục trong phòng tối. [4]
Sau nhiều thử nghiệm và thất bại (do ban đầu nhóm của Osamu tập trung tìm kiếm luciferin, có bản chất là những hợp chất hữu cơ kích thước nhỏ, trong khi khả năng phát sáng của loài sứa này lại do các protein đảm nhiệm), nhóm của ông đã thu nhận thành công hợp chất có hoạt tính phát quang, đó là một protein được đặt tên là aequorin, phát sáng khi có sự hiện diện của ion calcium. Để có được aequorin tinh sạch, Osamu đầu tiên thu nhận phần cơ quan phát sáng của sứa (phần rìa của cơ thể sứa), sau đó các mô và tế bào được phá vỡ bằng biên pháp cơ học (nghiền) để giải phóng tất cả các thành phần nội bào. Tất cả các protein trong mẫu được kết tủa bằng ammonium sulfate. Hỗn hợp protein sau đó được phân tách thành các phân đoạn khác nhau dựa trên khối lượng và điện tích bằng phương pháp sắc kí. Kế đến, Osamu xác định xem phân đoạn nào có khả năng phát sáng khi được bổ sung ion calcium (trước đó, ông đã nhận thấy sứa chỉ phát sáng khi trong môi trường có ion calcium). Từ đó, Osamu đã xác định được phân đoạn protein có chứa aequorin và tiếp tục thực hiện phương pháp sắc kí với phân đoạn này để thu được aequorin tinh sạch [7] [8]. Tuy nhiên, đó chưa phải là câu trả lời cho khả năng phát quang của sứa A. victoria do loài sứa này phát ra ánh sáng xanh lục trong khi aequorin phát sáng xanh lam. [9]
Trong quá trình tìm kiếm lời giải thực sự, Osamu đã thu nhận được một protein khác từ sứa, có khả năng phát huỳnh quang xanh, protein đó sau này được gọi là GFP (Green Fluorescent Protein – protein phát huỳnh quang xanh). Mối liên hệ giữa aequorin và GFP cũng được giải đáp khi ánh sáng xanh của aequorin có bước sóng (λ= 470 nm) gần bằng bước sóng trong khoảng kích thích của GFP (λ=460 nm). Do GFP là một chất phát huỳnh quang (hiện tượng một chất hấp thụ ánh sáng hoặc bức xạ điện từ có bước sóng lớn và phát xạ ánh sáng có bước sóng nhỏ hơn) nên đã hấp thụ ánh sáng do aequorin phát ra và phát xạ ánh sáng xanh lục. Sau khi hấp thụ năng lượng ánh sáng từ aequorin, GFP phát ra huỳnh quang có bước sóng khoảng 510 nm, nằm trong quang phổ xanh lục. Vì vậy, ánh sáng của sứa A. victoria chính là do GFP tạo ra. [9]
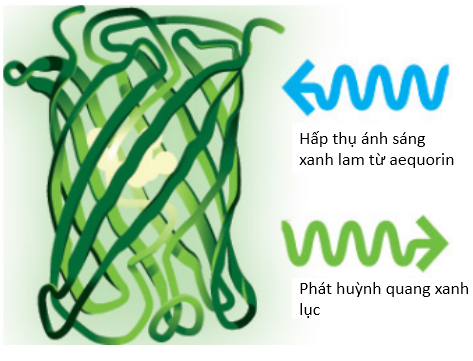
Hình 3: Cấu trúc ba chiều của GFP và cách GFP phát sáng. GFP là một protein có 238 amino acid, cấu trúc bậc ba bao gồm 11 phiến b xếp thành hình khối trụ, một xoắn a chạy dọc trong lòng và che phủ hai đầu khối trụ. [10]
Tuy cùng được phát hiện vào năm 1962, số phận của aequorin và GFP lại khá khác biệt nhau: do khả năng phát quang khi có sự hiện diện của ion calcium, một ion có vai trò quang trọng trong cơ thể sống, từ 1967, aequorin đã bắt đầu được ứng dụng trong các thí nghiệm về ảnh hưởng của ion này với sự sống, mức độ ứng dụng của aequorin đạt đến đỉnh điểm vào giữa thập kỉ 80. Ngược lại, người bà con của nó, GFP, lại bị xem như khá vô dụng trong vòng 30 năm kể từ khi được phát hiện. Điều này là do các nhà khoa học thời đó tin rằng GFP chỉ có thể phát sáng dưới sự giúp đỡ của các enzyme đặc biệt trong A. victoria. [4]
Nếu như Osamu Shimomura là người phát hiện ra GFP thì Martin Chalfie, cùng với sự giúp đỡ của Douglas Prasher là những người đã chứng minh cho thế giới thấy tiềm năng thực sự của GFP. Prasher, kết hợp thư viện bộ gene của A. victoria cũng như trình tự amino acid của GFP, đã xác định được một đoạn gene mã hóa cho một protein có kích thước 238 amino acid, bằng với kích thước GFP. Đồng thời, đoạn gene này còn mang đúng trình tự chromophore (là một nguyên tử hoặc nhóm nguyên tử quyết định màu sắc của hợp chất mang chromophore đó) của GFP. Chromophore của GFP được tạo thành từ 3 amino acid là serine, tyrosine và glycine ở các vị trí lần lượt là 65, 66, 67. Khi GFP gấp cuộn thành cấu trúc bậc ba, các amino acid này bị đẩy lại gần nhau, do ái lực tự nhiên của các nhóm bên trên các amino acid trên, chúng sẽ tự đóng vòng và trải qua các quá trình dehydro, dehydrat và oxi hóa để tạo thành cấu trúc chromophore hoàn chỉnh. Khi lần đầu tiên nghe về GFP vào năm 1988, Martin Chalfie, một nhà khoa học người Mĩ chuyên nghiên cứu về giun tròn Caenorhabditis elegans, cảm thấy vô cùng phấn khích. Công trình mà ông theo đuổi là tìm hiểu sự phát triển của hệ thần kinh giun tròn C. elegans, một loài sinh vật gần như trong suốt, vì vậy, ý tưởng kết hợp GFP với loài giun này lập tức lóe lên trong đầu Chalfie, việc có thể thấy được từng tế bào và thậm chí là các thành phần tế bào phát sáng trong một sinh vật sống là một ý tưởng hết sức hấp dẫn với Chalfie. Tuy nhiên, phải đến năm 1992, sau khi Prasher thành công trong việc thu được gene GFP hoàn chỉnh, Chalfie mới có thể tiến hành ước mơ của mình. Bằng cách kết hợp gene GFP với một gene có sẵn của C. elegans và sau đó chuyển vào trong giun tròn sống, Chalfie đã tạo ra được những cá thể C. elegans phát huỳnh quang xanh khi được kích thích trước đó bằng ánh sáng có bước sóng phù hợp (1994). Với kết quả này, ông không những có thể nghiên cứu tỉ mỉ hơn về C. elegans mà còn chứng minh được rằng GFP hoàn toàn có khả năng phát huỳnh quang tự thân mà không cần đến sự trợ giúp của bất kì enzyme hoặc chất hỗ trợ nào khác ngoài oxi. Nhưng ý nghĩa quan trọng nhất trong công trình của Chalfie là việc ông đã trao cho giới khoa học công cụ để bước sâu hơn vào thế giới của sinh học phân tử, sinh hóa và cả sinh học tế bào. Từ nay, các nhà nghiên cứu có thể “quan sát” những hoạt động, phản ứng đang diễn ra trong tế bào và cơ thể sống theo đúng nghĩa đen của từ “quan sát”. Sau thành công với C. elegans, GFP cũng đã được ứng dụng để phát huỳnh quang ở các loài sinh vật khác như vi khuẩn E. coli, nấm men S. cerevisiae, ruồi giấm D. melanogaster cũng như các loài động vật bậc cao hơn như cá ngựa vằn, chuột, thỏ,… [6] [9]
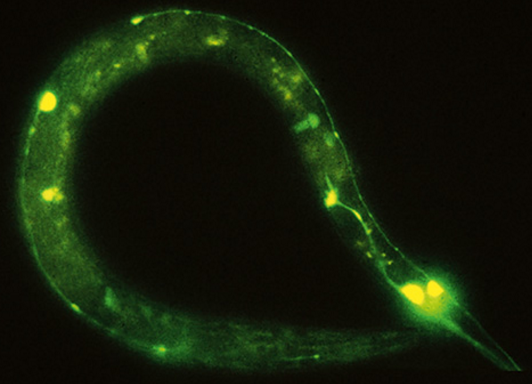
Hình 4: Một cá thể giun tròn C. elegans phát ánh sáng xanh sau khi được chuyển gene GFP. [10]
Như rất nhiều các công trình khoa học lớn khác, thành công trong việc tìm thấy và ứng dụng một hợp chất tự nhiên chỉ mới là bước khởi đầu. Nếu như các nhà sinh học là người đã khai phá tiềm năng của GFP, thì việc mở rộng ứng dụng của nó là nhiệm vụ của hóa học. Trong số những người nghiên cứu về GFP, Roger Yonchien Tsien (đại học California) là một trong những người thành công nhất. Là một nhà hóa học, ông tập trung nghiên cứu về cấu trúc và cơ chế hoạt động của GFP cũng như cách cải thiện nó. Chính Tsien và cộng sự đã phát hiện thấy oxi là nhân tố cần thiết cho sự hoàn thiện GFP trong tế bào cũng như cách mà nó phát sáng. Từ những hiểu biết về cơ chế hoạt động, trong khoảng thời gian từ năm 1994-1998, Tsien đã tạo ra rất nhiều những biến đổi trong trình tự amino acid của GFP, những biến đổi mà ông nghĩ sẽ có ảnh hưởng đến sự phát huỳnh quang của GFP. Nhiều thí nghiệm của Tsien đã thành công và thành quả là những dẫn xuất của GFP có khả năng hấp thụ và phát xạ ánh sáng ở nhiều bước sóng khác nhau cũng như cải thiện độ sáng và độ ổn định của các dẫn xuất này. [6] [9]
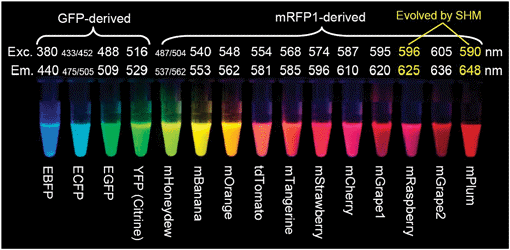
Hình 5: Các dẫn xuất phát sáng các màu sắc khác nhau của GFP và mRFP1 (một dẫn xuất nhân tạo được cải tiến từ protein phát huỳnh quang đỏ DsRed trong các loài san hô thuộc chi Discosoma. Exc: bước sóng kích thích của các dẫn xuất. Em: bước sóng phát xạ của các dẫn xuất. [11]
Vì những đóng góp của mình Osamu Shimomura, Martin Chalfie và Roger Yonchien Tsien đã được trao tặng giải Nobel hóa học 2008 vì “sự phát hiện và phát triển những hiểu biết về GFP”. Ngoài ra, nhiều ý kiến cũng cho rằng Douglas Prasher cũng xứng đáng với giải thưởng khi ông là người đầu tiên cô lập và thu nhận thành công gene mã hóa cho GFP cũng như cung cấp đoạn gene này cho các nhà khoa học khắp thế giới, trong đó có cả Chalfie và Tsien. Ông cùng với Chalfie đã thành công khi chứng minh khả năng phát sáng của GFP khi được biểu hiện ở E. coli. Tuy nhiên, Prasher sau đó phải từ bỏ việc theo đuổi nghiên cứu do khó khăn về tài chính cũng như quy định giải Nobel chỉ được trao cho tối đa 3 người khiến ông vuột mất cơ hội nhận được giải thưởng danh giá này. [12] [13]

Hình 6: Ba nhà khoa học được trao giải Nobel hóa học 2008.
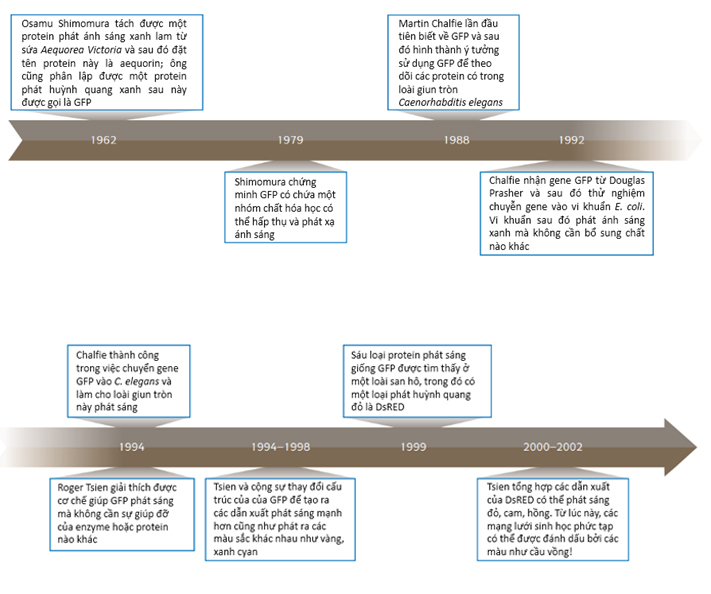
Hình 7: Các cột mốc quan trọng của ba nhà khoa học đạt giải Nobel hóa học 2008. [6]
Những phát kiến của lĩnh vực sinh hóa trong thế kỉ 20 đã giúp các nhà khoa học hiểu được những nguyên lí nền tảng của các quá trình chuyển hóa trong cơ thể sống, hiểu được cấu tạo và chức năng của các enzyme. Bên cạnh sinh hóa, thế kỉ 20 còn chứng kiến sự kết hợp của di truyền học và hiểu biết về bản chất hóa học nucleic acid, từ đó khai sinh ra khoa học nghiên cứu về bộ gene (genomics). Cuộc cách mạng trên cùng sự kết hợp với tin sinh học và các kĩ thuật phụ trợ (khuếch đại trình tự DNA, tổng hợp nhân tạo DNA…) đã giúp loài người giải trình tự toàn bộ bộ gene của nhiều loài, đóng góp cho sự phát triển của y dược và ung thư học. Tuy nhiên, cả hai lĩnh vực trên, sinh hóa và genomics, đều chưa cung cấp được một công cụ hiệu quả để định lượng và theo dõi ở mức độ phân tử các quá trình diễn ra trong cơ thể sống. Nhiều kiến thức thu thập được về các quá trình này là thông qua các thử nghiệm kiểm tra gián tiếp. Việc nhuộm màu mô, tế bào hoặc các thành phần tế bào để quan sát thường diễn ra trên các mẫu vật chết. Vì vậy công nghệ ứng dụng GFP xuất hiện cuối thế kỉ 20 đầu thế kỉ 21 như một cuộc cách mạng trong nghiên cứu khoa học: GFP có khả năng phát sáng khi có oxi (tham gia vào quá trình oxi hóa để hình thành chromophore hoàn chỉnh) và kích thích phù hợp; kích thước gene mã hóa GFP đủ nhỏ để dễ dàng thao tác và chuyển vào các tế bào muốn nghiên cứu; quan trọng nhất là GFP không ảnh hưởng đến hoạt động sinh học trong cơ thể sống và một khi đã chèn vào bộ gene, gene GFP có thể được di truyền qua nhiều thế hệ tế bào. Từ các đặc điểm đó, GFP giúp các nhà nghiên cứu trực tiếp thấy được cách mà sự sống diễn ra ở mức độ vi mô. Rất nhiều căn bệnh ở người đến từ những sai sót trong bộ máy làm việc của tế bào, GFP cũng chính là một trong những công cụ hiệu quả giúp chúng ta xác định được nguyên nhân của những sai sót đó. [9]
Nhờ sự phối hợp giữa nhiều yếu tố, từ đặc tính tự nhiên của GFP đến sự phát triển mạnh mẽ của kĩ thuật hình ảnh và phân tích dữ liệu, việc sử dụng GFP đã trở thành một phần vô cùng quan trọng trong nghiên cứu khoa học sự sống. Từ khi lần đầu được ứng dụng vào năm 1992 đến khi giải thưởng được trao năm 2008, đã có hơn 20 000 công trình nghiên cứu có liên quan đến GFP được công bố. Ứng dụng rộng rãi nhất của GFP là theo dõi vị trí, sự chuyển động và phản ứng hóa học liên quan đến các protein trong tế bào bằng cách kết hợp gene của protein muốn nghiên cứu với gene GFP. Các dẫn xuất phát quang khác nhau của GFP cho phép theo dõi nhiều loại protein khác nhau cùng một lúc trong cùng tế bào sống. [9]
Các ứng dụng khác của GFP như: nghiên cứu sự hoạt động của các gene; sự vận chuyển của các thành phần tế bào; nghiên cứu cấu trúc nhân tế bào; xây dựng các hệ thống cảm biến sinh học theo dõi các điều kiện nội bào như pH hoặc nồng độ các chất; quan sát các mô của sinh vật đa bào… [6] [9]
Với sự giúp đỡ của GFP, các nhà nghiên cứu đã có thể quan sát những quá trình vô hình như sự hư hại của các tế bào thần kinh của bệnh Alzheimer's, sự lan rộng của tế bào ung thư hay sự hình thành tế bào sinh insulin ở tụy của một bào thai đang phát triển. Đó chỉ là một vài ví dụ cho vô vàn những ứng dụng của GFP đang được các nhà nghiên cứu khắp thế giới khai thác. [3] [6]
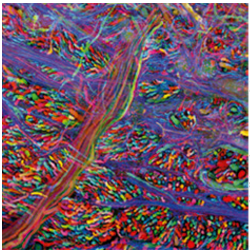
Hình 8: Một thí nghiệm ứng dụng các loại protein phát sáng dẫn xuất từ GFP: “The brainbow”: các tế bào não chuột được chuyển các gene mã hóa cho ba loại protein phát ánh sáng xanh lam, vàng và đỏ. Các gene phát huỳnh quang sẽ dung hợp với gene mã hóa các protein khác nhau trong tế bào. Các neuron khác nhau sẽ biểu hiện các protein với mức độ khác nhau. Khi các neuron biểu hiện protein đã được đánh dấu sẽ đồng thời biểu hiện protein phát huỳnh quang. Từ đó, mỗi tế bào sẽ có màu sắc khác nhau, thuận lợi cho việc quan sát tế bào cũng như nghiên cứu biểu hiện gene của của các neuron. [10]
Vậy, làm thế nào GFP có thể phát sáng ở cả sứa lẫn các loài sinh vật khác cũng như cách các nhà khoa học tạo ra những dẫn xuất đầy màu sắc của loại protein kì diệu này? Mời các bạn đón đọc kỳ 2: Câu chuyện của những Prometheus.
Tài liệu tham khảo:
|
[1] |
"Control of fire by early humans," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/Control_of_fire_by_early_humans. |
|
[2] |
"Thomas Edison," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/Thomas_Edison#Electric_light. |
|
[3] |
"The Nobel Prize in Chemistry 2008 - Press release," Nobelprize.org, 2008. [Online]. Available: https://www.nobelprize.org/nobel_prizes/chemistry/laureates/2008/press.html. |
|
[4] |
O. Shimomura, "Discovery of Green Fluorescent Protein (GFP) (Nobel lecture)," Angewandte Chemie, vol. 48, pp. 5590-5602, 2009. |
|
[5] |
"Molecular imaging," NARD institute, [Online]. Available: http://www.nard.co.jp/en/keyword/03_002.html. |
|
[6] |
"2008 nobel Laureates - The Nobel Prize in Chemistry 2008," 2008. [Online]. Available: https://www.nobelprize.org/nobel_prizes/nobelguide_che.pdf. |
|
[7] |
O. Shimomura, F. H. Johnson and Y. Saiga, "Extraction, purification and properties of aequorin, a bioluminescent protein from the luminous hydromedusan, Aequorea," Journal of cellular and comparative physiology, vol. 59, pp. 223-239, 1962. |
|
[8] |
"Extraction and purification of aequorin," European medical alliance, [Online]. Available: http://www.europeanmedical.info/resonance-energy/extraction-and-purification-of-aequorin.html. |
|
[9] |
M. Ehrenberg , "Scientific background on the Nobel Prize in Chemistry 2008 - The green fluorescent protein: discovery, expression and development," 2008. [Online]. Available: https://www.nobelprize.org/nobel_prizes/chemistry/laureates/2008/advanced-chemistryprize2008.pdf. |
|
[10] |
"The Nobel Prize in Chemistry 2008 - Illustrated presentation," Nobelprize.org, 2008. [Online]. Available: https://www.nobelprize.org/nobel_prizes/chemistry/laureates/2008/illpres.html. |
|
[11] |
R. Y. Tsien, "Constructing and exploiting the fluorescent protein paintbox," in The Nobel prize in chemistry 2008, Stockholm, 2008. |
|
[12] |
M. Chalfie, "GFP, lighting up life," in The Nobel prize in chemistry 2008, Stockholm, 2008. |
|
[13] |
"Douglas Prasher," Wikipedia, [Online]. Available: https://en.wikipedia.org/wiki/Douglas_Prasher. |


